题目内容
13.蛋白质是由多种氨基酸构成的极为复杂的化合物,丙氨酸(C3H7O2N)是其中的一种.以下对丙氨酸的认识错误的是( )| A. | 它是有机化合物 | |
| B. | 该化合物中碳、氢、氧、氮四种元素质量比为3:7:2:1 | |
| C. | 它是由碳、氢、氧、氮四种元素组成 | |
| D. | 它的相对分子质量为89 |
分析 A、根据有机化合物的概念来分析.
B、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
C、根据丙氨酸化学式的含义进行分析判断.
D、根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析判断.
解答 解:A.丙氨酸(C3H7O2N)是一种含碳的化合物,属于有机化合物,故正确;
B.丙氨酸中C、H、O、N四种元素质量比为(12×3):(1×7):(16×2):14=36:7:32:14,故错误;
C.丙氨酸是由碳、氢、氧、氮四种元素组成的,故正确;
D.丙氨酸的相对分子质量为12×3+1×7+16×2+14=89,故正确.
故选B.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
4. 已知:草酸钙(CaC2O4)是一种难溶于水的白色固体,受热易分解生成碳酸钙和一种有毒的气体;碳酸钙高温分解生成氧化钙和二氧化碳;草酸钙能与稀盐酸反应生成氯化钙和可溶于水的草酸(H2C2O4).相关反应的化学方程式为:CaC2O4+2HCl═CaCl2+H2C2O4
已知:草酸钙(CaC2O4)是一种难溶于水的白色固体,受热易分解生成碳酸钙和一种有毒的气体;碳酸钙高温分解生成氧化钙和二氧化碳;草酸钙能与稀盐酸反应生成氯化钙和可溶于水的草酸(H2C2O4).相关反应的化学方程式为:CaC2O4+2HCl═CaCl2+H2C2O4
(1)实验一:取一定量草酸钙固体,加热.加热过程中剩余固体的质量随时间变化如图所示.图中AB段发生反应的化学方程式为CaC2O4$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3+CO↑,
DE段固体所含物质为CaO,或氧化钙(写化学式或物质名称均可,下同).
(2)实验二:探究草酸钙加热一段时间后剩余固体M的成分.
(3)若加热前草酸钙的质量为6.4g,加热一段时间后剩余固体的质量为4.8g,则该固体中含有的物
质是碳酸钙和氧化钙.
 已知:草酸钙(CaC2O4)是一种难溶于水的白色固体,受热易分解生成碳酸钙和一种有毒的气体;碳酸钙高温分解生成氧化钙和二氧化碳;草酸钙能与稀盐酸反应生成氯化钙和可溶于水的草酸(H2C2O4).相关反应的化学方程式为:CaC2O4+2HCl═CaCl2+H2C2O4
已知:草酸钙(CaC2O4)是一种难溶于水的白色固体,受热易分解生成碳酸钙和一种有毒的气体;碳酸钙高温分解生成氧化钙和二氧化碳;草酸钙能与稀盐酸反应生成氯化钙和可溶于水的草酸(H2C2O4).相关反应的化学方程式为:CaC2O4+2HCl═CaCl2+H2C2O4(1)实验一:取一定量草酸钙固体,加热.加热过程中剩余固体的质量随时间变化如图所示.图中AB段发生反应的化学方程式为CaC2O4$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3+CO↑,
DE段固体所含物质为CaO,或氧化钙(写化学式或物质名称均可,下同).
(2)实验二:探究草酸钙加热一段时间后剩余固体M的成分.
| 步骤 | 实验操作 | 实验现象 | 实验结论 |
| Ⅰ | 取少量固体M放入烧杯中,向烧杯中加足量 水,充分搅拌后静置 | 杯底有白色固体,且温度无明显变化(填“有”或“无” | 固体M中不含氧化钙 |
| Ⅱ | 再向烧杯中加足量稀盐酸并不断搅拌 | 有气泡体产生,固体全部溶解. | 固体M中一定含有的物质是碳酸钙,可能含有草酸钙CaCO3. |
质是碳酸钙和氧化钙.
8.中国发射“天宫一号”的运载火箭使用的燃料是偏二甲肼,同时用四氧化二氮为氧化剂,两种物质反应的化学方程式为:2N2O4+R═4H2O+2CO2+3N2,则R的化学式是( )
| A. | C3H5O | B. | C2H5N5 | C. | C2H8 | D. | C2H8N2 |
5.葡萄糖(C6H12O6)属于( )
| A. | 混合物 | B. | 有机物 | C. | 单质 | D. | 氧化物 |
2.推理是化学学习中常用的思维方法.下列推理正确的是( )
| A. | 酸能使紫色石蕊溶液变红.通入CO2后的紫色石蕊溶液变红,所以CO2是酸 | |
| B. | 酸性溶液的pH小于7.食醋是酸性溶液,所以食醋的pH小于7 | |
| C. | 中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应 | |
| D. | 溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小 |
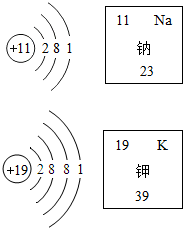 如图是两种原子的结构示意图和它在元素周期表中的部分信息,完成下列问题.
如图是两种原子的结构示意图和它在元素周期表中的部分信息,完成下列问题.