题目内容
13.某兴趣小组对物质的性质进行相关探究.【提出问题】氯化氢(HCl)气体显酸性吗?
【进行实验】该兴趣小组的同学根据二氧化碳与水反应的实验探究方法,用三朵由紫甘蓝的汁液染成蓝紫色的纸质干燥小花进行如图1的三个实验:
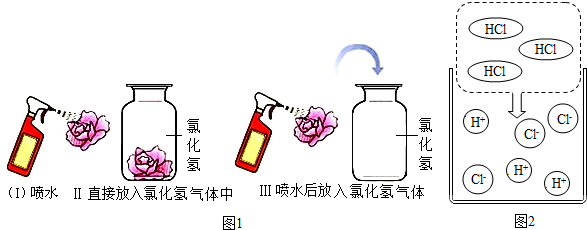
实验现象:I 和Ⅱ中小花不变色;Ⅲ中小花变红色.
【查阅资料】图 2 是同学们查阅的氯化氢气体溶于水的示意图.
【实验结论】氯化氢气体不显酸性.
【交流思想】
(1)紫色石蕊在酸性溶液中显红色.小明向实验Ⅲ中变红的小花上喷足量的稀氢氧化钠溶液,发现小花最后变成色,写出相关反应的化学方程式NaOH+HCl=NaCl+H2O.
(2)微观角度分析氯化氢气体不显酸性的原因是在氯化氢气体中,氯化氢以分子形式存在,没有解离出氢离子,所以氯化氢气体不显酸性.
(3)下列实验可以用来说明氯化氢气体不显酸性的是B.
A.测试盐酸的导电性,盐酸能导电 B.干燥的碳酸钠粉末放人氯化氢气体中,不反应
C.氢气与氯气反应,生成氯化氢气体.干燥的碳酸钠粉末放人盐酸中,能反应
(4)下列物质能用来干燥氯化氢气体的是D.
A.苛性钠 B.生石灰 C.石灰石 D.浓硫酸.
分析 (1)根据石蕊试液在酸碱性所显示的不同颜色以及反应的实质来分析;
(2)根据氯化氢气体是由氯化氢分子构成的进行分析;
(3)根据碳酸钠粉末遇到酸性物质会生成二氧化碳进行解答;
(4)氯化氢气体溶于水形成盐酸,不能用碱性物质来干燥.
解答 解:(1)向实验Ⅲ中变红的小花上喷足量的稀氢氧化钠溶液,将酸中和后,还显碱性,故显示蓝色;氢氧化钠溶液和盐酸反应生成氯化钠和水,故填:蓝;NaOH+HCl=NaCl+H2O;
(2)氯化氢气体是由氯化氢分子构成的,没有解离出的氢离子,所以氯化氢气体不显酸性,故填:在氯化氢气体中,氯化氢气体是由氯化氢分子构成的,没有解离出的氢离子,所以氯化氢气体不显酸性;故填:在氯化氢气体中,氯化氢以分子形式存在,没有解离出氢离子,所以氯化氢气体不显酸性;
(3)碳酸钠粉末遇到酸性物质会生成二氧化碳,所以干燥的碳酸钠粉末放入氯化氢气体中,不反应,说明氯化氢气体不显酸性,故填:B;
(4)苛性钠就是氢氧化钠,是一种碱,能与盐酸反应,生石灰是氧化钙也能与盐酸反应,碳酸钙与盐酸能反应,浓硫酸不与其反应,可做氯化氢气体的干燥剂.故填:D.
点评 在解此类题时,首先要了解题中的各个问题,然后将这些问题对准学过的知识点,再结合题中的要求各个突破.

练习册系列答案
相关题目
3.把氯化钙溶液加入到含有大量下列离子的溶液中,最终会得到无色澄清溶液的是( )
| A. | Na+ CO32-OH- | B. | Ag+ NO3- NH4+ | ||
| C. | K+ Cu2+NO3- | D. | SO42-NO3- H+ |
4.区分下列各组物质,所加试剂或操作方法错误的是( )
| 选项 | 待区分的物质 | 所加试剂或操作方法 |
| A | 白醋和水 | 闻气味 |
| B | 硬水和软水 | 加肥皂水 |
| C | 自来水和矿泉水 | 观察颜色 |
| D | 合成纤维和纯羊毛 | 取少量灼烧,并闻气味 |
| A. | A | B. | B | C. | C | D. | D |
8.化学中常常出现“1+1≠2”的有趣现象,但也有例外,下列符合“1+1=2”的事实是( )
| A. | 10g 硫粉在 10g 氧气中完全燃烧后生产 20g 二氧化硫 | |
| B. | 10L 水与 10L 酒精混合后的体积等于 20L | |
| C. | 10g 锌片与 10g 稀硫酸充分反应后所得的溶液质量为 20g | |
| D. | 25℃,10g 氯化钠饱和溶液中加入 10g 氯化钠固体能得到 20g 氯化钠溶液 |
5.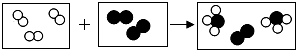 用“
用“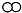 ”和“
”和“ ”分别代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生化学反应生成新物质X,微观过程如图所示.下列说法正确的是( )
”分别代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生化学反应生成新物质X,微观过程如图所示.下列说法正确的是( )
 用“
用“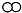 ”和“
”和“ ”分别代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生化学反应生成新物质X,微观过程如图所示.下列说法正确的是( )
”分别代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生化学反应生成新物质X,微观过程如图所示.下列说法正确的是( )| A. | 反应前后分子种类不发生改变 | |
| B. | 该反应为置换反应 | |
| C. | 参加反应的A2与B2分子数之比为 3:l | |
| D. | 物质X含4种元素 |
2.肉毒碱(C7H15NO3)被认为是“最佳减肥营养素”,关于它的说法正确的是( )
| A. | 相对分子质量为161g | |
| B. | 氢元素质量分数小于氮元素质量分数 | |
| C. | 含有臭氧(O3) | |
| D. | 分子中C、H、O、N原子个数比为7:15:3:1 |

 控制化学反应的条件可以促进或抑制化学反应,更好使化学反应为人类造福.
控制化学反应的条件可以促进或抑制化学反应,更好使化学反应为人类造福.
