题目内容
8.化学中常常出现“1+1≠2”的有趣现象,但也有例外,下列符合“1+1=2”的事实是( )| A. | 10g 硫粉在 10g 氧气中完全燃烧后生产 20g 二氧化硫 | |
| B. | 10L 水与 10L 酒精混合后的体积等于 20L | |
| C. | 10g 锌片与 10g 稀硫酸充分反应后所得的溶液质量为 20g | |
| D. | 25℃,10g 氯化钠饱和溶液中加入 10g 氯化钠固体能得到 20g 氯化钠溶液 |
分析 A、由于分子之间存在间隙,液体与液体相互混合时,其体积不能相加,即混合后液体体积不等于丙液体的体积和;
B、饱和溶液是在一定温度下一定量水中不能再继续溶解该溶质的溶液.
C、镁可以与稀盐酸反应生成氯化镁和氢气,在反应中镁与盐酸的质量比为24:73;
D、硫在氧气中燃烧生成二氧化硫,在反应中两物质的质量比为32:32,即两物质质量比为1:1时恰好完全反应.
解答 解:A、硫在氧气中燃烧生成二氧化硫,根据反应的化学方程式中两物质的质量关系32:32可知,10g硫粉在l0g氧气中燃烧恰好完全反应,根据质量守恒定律,反应后生成20g二氧化硫;故正确;
B、由于分子之间存在间隙,10L水与10L酒精混合后所得混合液体的体积小于20L;故不正确;
C、锌与稀硫酸反应生成硫酸镁和氢气,根据反应的化学方程式中两物质的质量关系65:98可知,10g稀硫酸不能完全消耗10g锌且放出气体氢气,利用质量守恒定律,可判断10g锌与10g稀硫酸充分反应后所得的溶液质量小于20g;故不正确;
D、向25℃的10g饱和氯化钠溶液中加入氯化钠10g,氯化钠的饱和溶液溶液不能继续溶解氯化钠,溶液的质量不变仍为10g;故不正确.
故选A.
点评 质量守恒定律指参加反应的物质质量总和与生成物质的质量总和相等;在化学反应中,只有反应物间的质量关系符合反应中物质间的质量比时,物质都好恰好完全反应.

练习册系列答案
相关题目
16.分析推理是化学学习中常用的思维方法.下列分析推理正确的是( )
| A. | 浓硫酸具有吸水性,所以浓盐酸也具有吸水性 | |
| B. | O2和O3的分子构成不同,所以它们的化学性质不同 | |
| C. | 碱的溶液显碱性,所以显碱性的溶液一定是碱溶液 | |
| D. | 成语“火上浇油”是指“油”可以使可燃物与氧气隔绝,达到灭火的目的 |
3. 红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸 剂”固体样品很好奇,设计实验进行探究.
红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸 剂”固体样品很好奇,设计实验进行探究.
【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.久置固体中可能含有Ca(OH)2的原因是(用化学方程式表示)CaO+H2O═Ca(OH)2.
【实验探究1】请你完成“甲同学方案”的表格. 甲同学的方案:
【实验质疑】
(1)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,还需要经过其他的定量实验进一步验证,理由是氧化钙和水反应能生成氢氧化钙,滴加无色酚酞溶液后溶液一定会变为红色,因此不能证明固体中有氢氧化钙.
(2)丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是氧化铁和盐酸反应生成的氯化铁,可能会继续与铁反应生成氯化亚铁,因此不能说明固体中一定没有Fe2O3.
【实验探究2】
丙同学认为可以先利用物理方法除去铁,再利用化学方法检验氧化铁的存在.请你帮他设计实验方案验证Fe2O3是否存在(写出实验步骤、现象和结论):取样,用磁铁充分吸引,再加入足量盐酸,若固体溶解,溶液变黄,则含有氧化铁.反之,则不含.
 红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸 剂”固体样品很好奇,设计实验进行探究.
红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸 剂”固体样品很好奇,设计实验进行探究.【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.久置固体中可能含有Ca(OH)2的原因是(用化学方程式表示)CaO+H2O═Ca(OH)2.
【实验探究1】请你完成“甲同学方案”的表格. 甲同学的方案:
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红. | 固体中一定含有CaO 和氢氧化钙. |
| (2)另取少量固体放于试管中,滴加足量的盐酸. | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有Fe, 一定不含Fe2O3. |
| (3)将步骤(2)中产生的气体通入到澄清的石灰水中. | 石灰水变浑浊. | 固体中一定含有CaCO3. |
(1)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,还需要经过其他的定量实验进一步验证,理由是氧化钙和水反应能生成氢氧化钙,滴加无色酚酞溶液后溶液一定会变为红色,因此不能证明固体中有氢氧化钙.
(2)丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是氧化铁和盐酸反应生成的氯化铁,可能会继续与铁反应生成氯化亚铁,因此不能说明固体中一定没有Fe2O3.
【实验探究2】
丙同学认为可以先利用物理方法除去铁,再利用化学方法检验氧化铁的存在.请你帮他设计实验方案验证Fe2O3是否存在(写出实验步骤、现象和结论):取样,用磁铁充分吸引,再加入足量盐酸,若固体溶解,溶液变黄,则含有氧化铁.反之,则不含.
20.下列归纳和总结完全正确的一组是( )
| A对鉴别的认识 | B食品安全 |
| ①灼烧闻气味,区分羊毛和尼龙 ②加水溶解,区分碳酸钙和硫酸钡 ③和熟石灰混合研磨闻气味,区分NH4Cl和CO(NH2)2 | ①霉变的大米洗净烧熟后可以食用 ②利用甲醛水溶液浸泡水产品防腐 ③补充维生素A防止夜盲症 |
| C对现象的认识 | D化学学科的价值 |
| ①花香四溢,说明分子在不断运动 ②铁在氧气中剧烈燃烧,产生红色固体 ③电解水生成氢气和氧气的体积比为2:1 | ①研制高效低毒农药,保障粮食生产 ②开发新型材料,改善人类生存条件 ③利用化学合成药物,保障人体健康 |
| A. | A | B. | B | C. | C | D. | D |
17.下列有关溶液性质的叙述中错误的是( )
| A. | 溶液一定是无色、透明的混合物 | |
| B. | 一种溶质的饱和溶液仍然可以溶解其它溶质 | |
| C. | 食盐水能导电是因为食盐水中含有自由移动的离子 | |
| D. | 海水是盐溶液,所以冬天海水不易结冰 |
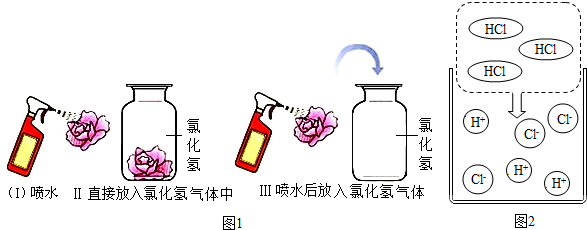
 某研究性学习小组设计并进行了如下实验.
某研究性学习小组设计并进行了如下实验.