题目内容
11.有一块表面被氧化的镁若干克与100g、质量分数为14.6%的稀盐酸恰好完全反应,产生0.2g气体.求:(1)原混合物中镁元素的质量分数;
(2)反应后溶液中溶质的质量分数.
分析 考虑氧化镁和稀盐酸反应生成氯化镁和水,镁和稀盐酸反应生成氯化镁和氢气,
根据生成氢气的质量可以计算镁的质量,进一步可以计算氧化镁的质量,从而可以计算反应后所得溶液的溶质质量分数.
解答 解:设镁的质量为x,参与反应的HCl质量为y,生成氯化镁的质量为z,
Mg+2HCl═MgCl2+H2↑,
24 73 95 2
x y z 0.2g
则$\frac{24}{x}=\frac{73}{y}=\frac{2}{0.2g}$=$\frac{95}{z}$,解得x=2.4g,y=7.3g,z=9.5g.
则与氧化镁反应的HCl质量为100g×14.6%-7.3g=7.3g.
设氧化镁和稀盐酸反应的质量氧化镁为a,生成氯化镁的质量为b.
MgO+2HCl═MgCl2+H2O,
40 73 95
a 7.3g b
则$\frac{40}{a}=\frac{73}{7.3g}=\frac{95}{b}$,解得a=4.0g,b=9.5g.
答:(1)原混合物中镁元素的质量分数$\frac{2.4g+4.0g×(\frac{24}{40}×100%)}{2.4g+4.0g}×100%$=75%;
(2)反应后所得溶液的溶质质量分数为:$\frac{9.5g+9.5g}{2.4g+4.0g+100g-0.2g}$×100%=17.9%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
2.通过下列实验得出的结论中,正确的是( )
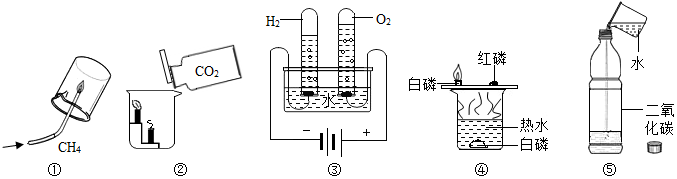
①可说明甲烷是由氢元素和碳元素组成
②可说明二氧化碳的密度比空气大,且二氧化碳不能燃烧也不支持燃烧
③可说明水是由氢元素、氧元素组成
④可说明白磷的着火点比红磷低
⑤可说明二氧化碳具有酸性.

①可说明甲烷是由氢元素和碳元素组成
②可说明二氧化碳的密度比空气大,且二氧化碳不能燃烧也不支持燃烧
③可说明水是由氢元素、氧元素组成
④可说明白磷的着火点比红磷低
⑤可说明二氧化碳具有酸性.
| A. | ①②③④ | B. | ②③④ | C. | ②③④⑤ | D. | ①②③④⑤ |
3.下列各方程式中,书写正确是( )
| A. | 2P+5O2═P2O5 | B. | 4Fe+3O2 $\frac{\underline{\;点燃\;}}{\;}$2 Fe2O3 | ||
| C. | C2H5OH+3O2 $\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O | D. | C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2 |

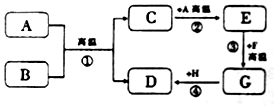 A-H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,它们的转化关系如图所示,请回答:
A-H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,它们的转化关系如图所示,请回答: