题目内容
12.工业烧碱具有较好的杀菌消毒作用且廉价易得,但工业烧碱遇空气容易变质,使其常含有杂质碳酸钠.某科学学习小组同学围绕工业烧碱样品纯度测定问题,展开了讨论与探究.(1)他们的测定方案是:利用Na2CO3与稀H2SO4反应产生CO2,通过CO2质量的测定,确定样品中碳酸钠的质量,从而计算样品中烧碱的纯度.装置如图所示,请问:此方案中二氧化碳质量的测定方法是:称量C装置在反应前后质量的变化,增加的质量就是二氧化碳质量.
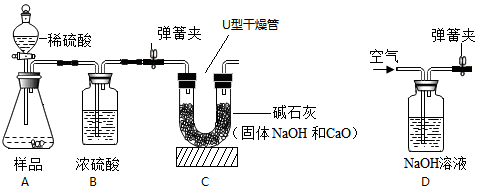
(2)有同学认为上述实验方案会导致二氧化碳质量测定的不准确,准备在如图A装置前连接D装置,在反应前、后都要同一定量的空气.他这样设计的目的是CD.
A.为了检验装置的气密性
B.为了加入的稀硫酸与样品反应更充分
C.反应前通空气是为了排尽装置内原有空气中的二氧化碳
D.反应后通空气是为了排尽装置内生成的二氧化碳
(3)为了使测定的二氧化碳质量更准确,准备在如图A装置前连接D装置.大家认为有道理.若没有这装置,则测得工业烧碱的纯度将偏低(填“偏高”“偏低”或“无影响”)
分析 (1)称量C装置在反应前后质量的变化,增加的质量就是二氧化碳质量.
(2)反应前通空气是为了排尽装置内原有空气中的二氧化碳,反应后通空气是为了排尽装置内生成的二氧化碳,将生成的二氧化碳全部被C装置吸收.
(3)若没有在A装置前连接D装置,会导致测得二氧化碳的质量偏小.
解答 解:(1)此方案中二氧化碳质量的测定方法是称量C装置在反应前后质量的变化,增加的质量就是二氧化碳质量,故填:称量C装置在反应前后质量的变化,增加的质量就是二氧化碳质量.
(2)在如图A装置前连接D装置,在反应前、后都要通一定量的空气,反应前通空气是为了排尽装置内原有空气中的二氧化碳,反应后通空气是为了排尽装置内生成的二氧化碳,将生成的二氧化碳全部被C装置吸收.故选CD.
(3)若没有在A装置前连接D装置,会导致测得二氧化碳的质量偏小,测得工业烧碱的纯度将偏低,故填:偏低.
点评 解答这类题目时,首先,赏析问题情景,找到实验探究的反应原理;再根据实验的反应原理,分析推断出该物质的组成成分,然后得出所要探究的物质中该成分的组成.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目
8. 物质的组成、结构及变化是化学研究的主要问题之一.
物质的组成、结构及变化是化学研究的主要问题之一.
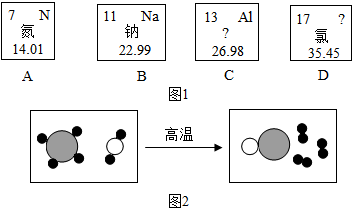
(1)如图1所示是从元素周期表中截取的四种元素的信息,请回答下列问题:
①C元素的一种微粒的结构示意图为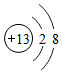 它属于金属元素(填“金属元素”或“非金属元素”或“稀有气体元素”),该微粒的符号为Al3+;
它属于金属元素(填“金属元素”或“非金属元素”或“稀有气体元素”),该微粒的符号为Al3+;
②由B与D形成化合物的化学式是NaCl.
(2)在一密闭容器内有氧气、二氧化碳、水蒸气和一种未知物W,在一定条件下充分反应,测得反应前后各物质的质量如表所示.
①X的数值为0.
②W中含有的元素是碳、氢、氧.
(3)如图2所示是工业上制备氢气的微观示意图,其中不同的“球”代表不同的原子.下列说法不正确的是AC(填字母序号).
A.反应前后,分子个数不变
B.反应前后,原子的种类、数目不变
C.该反应中共涉及两种单质和三种化合物
D.该反应中参加反应的两种分子的个数比为1:1.
 物质的组成、结构及变化是化学研究的主要问题之一.
物质的组成、结构及变化是化学研究的主要问题之一.(1)如图1所示是从元素周期表中截取的四种元素的信息,请回答下列问题:
①C元素的一种微粒的结构示意图为
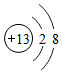 它属于金属元素(填“金属元素”或“非金属元素”或“稀有气体元素”),该微粒的符号为Al3+;
它属于金属元素(填“金属元素”或“非金属元素”或“稀有气体元素”),该微粒的符号为Al3+;②由B与D形成化合物的化学式是NaCl.
(2)在一密闭容器内有氧气、二氧化碳、水蒸气和一种未知物W,在一定条件下充分反应,测得反应前后各物质的质量如表所示.
| 物 质 | 氧 气 | 二氧化碳 | 水蒸气 | W |
| 反应前质量/g | 50 | 1 | 1 | 23 |
| 反应后质量/g | 2 | 45 | 28 | x |
②W中含有的元素是碳、氢、氧.
(3)如图2所示是工业上制备氢气的微观示意图,其中不同的“球”代表不同的原子.下列说法不正确的是AC(填字母序号).
A.反应前后,分子个数不变
B.反应前后,原子的种类、数目不变
C.该反应中共涉及两种单质和三种化合物
D.该反应中参加反应的两种分子的个数比为1:1.
4.下列属于化学研究范畴的是( )
| A. | 从棉花纺成纱到制成布的工艺 | B. | 新能源的开发和新材料的研制 | ||
| C. | “神七”飞船轨道的研究 | D. | 动植物细胞的组成和结构 |
1.下列描述属于氧气化学性质的是( )
| A. | 通常状况下,氧气是无色、无味的气体 | |
| B. | 通过低温加压,可使氧气液化成淡蓝色的液体 | |
| C. | 氧气可用于潜水 | |
| D. | 氧气是一种性质比较活泼的气体,能氧化许多物质 |
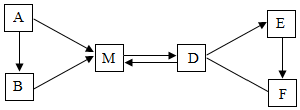 A、B、D、E、F、M是初中化学的常见六种物质.A、B组成元素相同,B是一种液态氧化物,M是气体单质,D是一种由剧毒的气体,E是红色金属单质,F是与E有相同元素的黑色固体.它们之间有如图转化关系:(图中“→”表示能生成,“-”表示能互相反应,其他反应物和反应条件省略)
A、B、D、E、F、M是初中化学的常见六种物质.A、B组成元素相同,B是一种液态氧化物,M是气体单质,D是一种由剧毒的气体,E是红色金属单质,F是与E有相同元素的黑色固体.它们之间有如图转化关系:(图中“→”表示能生成,“-”表示能互相反应,其他反应物和反应条件省略)