题目内容
5.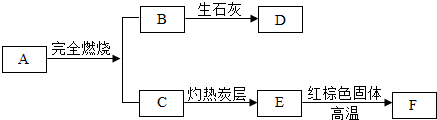 A~F是初中化学中的常见物质,如图是它们之间的转化关系,图中部分反应物或生成物未全部标出.已知:A是天然气的主要成分,B在常温下为液态,F是黑色粉末.
A~F是初中化学中的常见物质,如图是它们之间的转化关系,图中部分反应物或生成物未全部标出.已知:A是天然气的主要成分,B在常温下为液态,F是黑色粉末.(1)B→D是放热反应(填“放热”或“吸热”);
(2)C→E属于基本反应类型中的化合反应;
(3)写出A完全燃烧的化学方程式:CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$ CO2+2H2O
(4)写出E→F的化学反应方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(5)写出E物质的另一种用途用作燃料.
分析 根据已有的知识进行分析,根据“A是天然气的主要成分”,则A是甲烷,甲烷完全燃烧生成二氧化碳和水,根据“B在常温下为液态”,则B是水,C是二氧化碳,水能与氧化钙反应生成氢氧化钙,同时放出大量的热,则D是氢氧化钙;二氧化碳能与灼热的碳反应生成一氧化碳,则E是一氧化碳,一氧化碳具有还原性,能还原金属氧化物;红棕色固体可能是氧化铁,则生成的黑色粉末F是铁,据此解答.
解答 解:根据已有的知识进行分析,根据“A是天然气的主要成分”,则A是甲烷,甲烷完全燃烧生成二氧化碳和水,根据“B在常温下为液态”,则B是水,C是二氧化碳,水能与氧化钙反应生成氢氧化钙,同时放出大量的热,则D是氢氧化钙;二氧化碳能与灼热的碳反应生成一氧化碳,则E是一氧化碳,一氧化碳具有还原性,能还原金属氧化物;红棕色固体可能是氧化铁,则生成的黑色粉末F是铁,代入框图,推断合理;
(1)B→D是氧化钙与水反应,此反应是放热反应,故填:放热;
(2)C是二氧化碳,与碳在高温下反应生成一氧化碳,是化合反应,故填:化合;
(3)A完全燃烧的化学方程式:CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$ CO2+2H2O;
(4)E是一氧化碳,能与氧化铁反应生成铁和二氧化碳,故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(5)一氧化碳还具有可燃性,能用作燃料,故填:燃料.
故答案为:
(1)放热;(2)化合反应;(3)CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$ CO2+2H2O;
(4)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;(5)用作燃料
点评 本题为框图式物质推断题,完成此题的关键是根据题干叙述,找准解题突破口,直接得出有关物质的化学式,然后推断得出其他物质的化学式,书写反应的化学方程式要注意配平.

| 序号 | 样品成分 | 所选试剂 | 操作方法 |
| A | KCl(MnO2) | 水 | 溶解、过滤、洗涤、干燥 |
| B | Na2CO3(NH4HCO3) | / | 加热至质量不再减少 |
| C | NaCl(KNO3) | 水 | 溶解、降温结晶、过滤 |
| D | NaCl(CuCl2) | 过量NaOH溶液 | 过滤、蒸发结晶 |
| A. | A | B. | B | C. | C | D. | D |
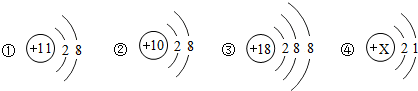
| A. | ①②④ | B. | ①② | C. | ②④ | D. | 无法判断 |
| A. | 水溶解时放出大量的热 | B. | 对皮肤有强列的腐蚀作用 | ||
| C. | 水溶液能使石蕊溶液变红 | D. | 把水注入浓硫酸中,将浓硫酸稀释 |
| A. |  加热固体 | B. |  加热液体 | C. |  振荡试管 | D. |  加热蒸发 |


 在化学游戏上,小明在圆形卡片上填上不同的物质,摆成一个五连环(如图),让相邻物质在常温下能发生反应.小明对其他同学提出下列问题,请你参与:
在化学游戏上,小明在圆形卡片上填上不同的物质,摆成一个五连环(如图),让相邻物质在常温下能发生反应.小明对其他同学提出下列问题,请你参与: