题目内容
15.某中学科学兴趣小组按照图甲的实验方法,做木炭与氧化铜反应实验时,虽然澄清石灰水能变浑浊,但是很难观察到紫红色铜的生成,却往往有暗红色固体出现.暗红色的固体是什么?怎样使现象更明显呢?他们决定对这个实验进行进一步的探究
查阅资料后,获知铜有+1和+2两种化合价
(1)小敏认为这种暗红色固体可能是一种化合物,并猜测它的化学式为Cu2O.他猜想的依据之一是生成物的颜色,另一依据是铜有+1和+2两种化合价,通常情况下,氧的化合价为-2,根据化合物中元素的化合价代数和为零的原则.写出按小敏猜想的反应方程式4CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu2O+CO2↑
(2)小王建议用超细炭粉与氧化铜粉末进行实验.可使实验现象更明显,她提出这样建议的原理是增大接触面积,促进充分反应.
(3)在小王的基础上,小新建议将实验方案作如图乙的改进(酒精喷灯能提供更多的热量):并待反应结束时,先将导气管从石灰水中取出,然后关闭止水夹,让产物自然冷却.若不关闭止水夹,可能出现的问题是使生成的依然灼热的铜重新被氧化.待产物冷却后,同学们终于获得了紫红色铜,实验获得了圆满成功.
分析 在明确探究目的在基础上,仔细阅读所给的信息,猜测化学式时应根据化合物中元素的化合价代数和为零的原则;物质接触面积越大反应就越充分,用超细炭粉与氧化铜粉末反应是合理的;反应结束后要关闭止水夹,防止进入空气,使灼热的铜再被氧化
解答 解:(1)因为铜有+1和+2两种化合价,通常情况下,氧的化合价为-2,根据化合物中元素的化合价代数和为零的原则,暗红色固体的化学式可能为:Cu2O
反应的方程式为:4CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu2O+CO2↑;
(2)乙装置中超细炭粉与氧化铜粉末进行,增大接触面积,促进充分反应;
(3)反应结束后要关闭止水夹,防止进入空气,使灼热的铜再被氧化.
故答案为:(1)铜有+1和+2两种化合价,通常情况下,氧的化合价为-2,根据化合物中元素的化合价代数和为零的原则;4CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu2O+CO2↑;
(2)是有利于集中加热,获得持续高温(3)使生成的依然灼热的铜重新被氧化
点评 完成实验探究题时,要明确探究的目的,根据所给信息按步骤进行分析,认真思考反应中的现象,不放过细节问题

练习册系列答案
相关题目
16.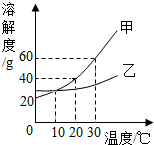 如图是甲、乙两种固体物质的溶解度曲线.下列有关叙述不正确的是( )
如图是甲、乙两种固体物质的溶解度曲线.下列有关叙述不正确的是( )
 如图是甲、乙两种固体物质的溶解度曲线.下列有关叙述不正确的是( )
如图是甲、乙两种固体物质的溶解度曲线.下列有关叙述不正确的是( )| A. | 20℃时,甲物质的溶解度为40g | |
| B. | 10℃时,甲、乙两种物质的溶解度相等 | |
| C. | 30℃时,甲物质饱和溶液的质量分数为60% | |
| D. | 除去甲物质中少量乙物质可采取蒸发结晶的方法 |
10.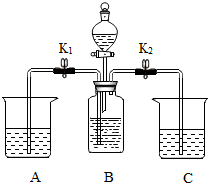 实验是学习化学的重要手段之一.某班同学分成两个小组,利用如图所示装置进行如下实验,请你参与他们的实验过程.
实验是学习化学的重要手段之一.某班同学分成两个小组,利用如图所示装置进行如下实验,请你参与他们的实验过程.
 实验是学习化学的重要手段之一.某班同学分成两个小组,利用如图所示装置进行如下实验,请你参与他们的实验过程.
实验是学习化学的重要手段之一.某班同学分成两个小组,利用如图所示装置进行如下实验,请你参与他们的实验过程.| 第一小组同学的实验: | 第二小组同学的实验: | |||||||||
| 位置 | A | B | C | 分液漏斗 | 位置 | A | B | C | 分液漏斗 | |
| 药品 | 澄清石灰水 | 碳酸钠溶液 | 澄清石灰水 | 稀盐酸 | 药品 | X溶液 | 稀盐酸 | 水(滴有石蕊溶液) | 碳酸钠溶液 | |
| 操作 | 关闭K1,打开K2和分液漏斗的活塞, 缓慢滴加稀盐酸 | 操作 | 关闭K1,打开K2和分液漏斗的活塞, 缓慢滴加碳酸钠溶液 | |||||||
| 现象,并写出C中反应化学方程式 | (1) B中有气泡产生,C中澄清石灰水变浑浊 (2) Ca(OH)2+CO2═CaCO3↓+H2O | 现象 | (3) B中有大量的气泡产生,C中紫色石蕊变红 | |||||||
| 操作 | 关闭K2,打开K1 | 操作 | 关闭K2,打开K1 | |||||||
| 现象 | B中液体沿导管流入A中, A中有白色沉淀产生 | 现象 | B中液体沿导管流入A中, A中有无色气体产生 | |||||||
| 上述现象产生的原因 | (4) B中不断产生CO2,压强增大,将B中碳酸钠溶液压入A中,和A中的澄清石灰水发生反应,生成碳酸钙白色沉淀 | 写出A中X溶液的溶质 | 至少写两种:(5) Na2CO3、NaHCO3 | |||||||
7.下列区分物质的方法中不正确的是( )
| A. | 熟石灰和烧碱:用水,观察是否放热 | |
| B. | 石灰水与氢氧化钠溶液:滴加酚酞溶液,看是否变色 | |
| C. | 黄金与黄铜(铜锌合金):滴加稀盐酸,观察是否有气泡产生 | |
| D. | 硫酸铜溶液和氯化铁溶液:用观察法 |
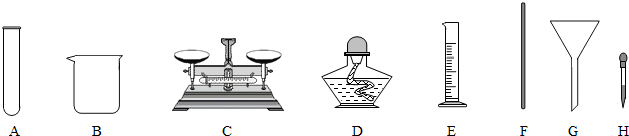 (1)配制时,在上面的仪器中除B、C、E外,还必须选用的是(填字母编号)FH.
(1)配制时,在上面的仪器中除B、C、E外,还必须选用的是(填字母编号)FH.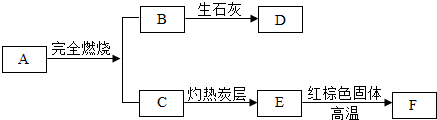 A~F是初中化学中的常见物质,如图是它们之间的转化关系,图中部分反应物或生成物未全部标出.已知:A是天然气的主要成分,B在常温下为液态,F是黑色粉末.
A~F是初中化学中的常见物质,如图是它们之间的转化关系,图中部分反应物或生成物未全部标出.已知:A是天然气的主要成分,B在常温下为液态,F是黑色粉末.