题目内容
16.为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
(1)步骤①⑤⑦中都用到的一种玻璃仪器为玻璃棒.
(2)判断BaCl2已过量的方法是取少量上层清液,滴加硫酸钠,若不产生白色沉淀,则证明氯化钡已经过量.
(3)第④步中,相关的化学方程式有BaCl2+Na2CO3=BaCO3↓+2NaCl,CaCl2+Na2CO3=CaCO3↓+2NaCl.
分析 (1)根据溶解、过滤、蒸发需要的玻璃仪器进行分析;
(2)根据钡离子和硫酸根离子会生成硫酸钡沉淀进行分析;
(3)根据碳酸钠与氯化钡反应生成碳酸钡沉淀和氯化钠,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠进行分析.
解答 解:(1)溶解时需要的玻璃仪器有烧杯、玻璃棒,过滤时需要的玻璃仪器有烧杯、漏斗、玻璃棒,蒸发需要的玻璃仪器有玻璃棒,所以步骤①⑤⑦中都用到的一种玻璃仪器为玻璃棒;
(2)钡离子和硫酸根离子会生成硫酸钡沉淀,所以检验的方法是:取少量上层清液,滴加硫酸钠,若不产生白色沉淀,则证明氯化钡已经过量;
(3)碳酸钠与氯化钡反应生成碳酸钡沉淀和氯化钠,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,化学方程式为:BaCl2+Na2CO3=BaCO3↓+2NaCl,CaCl2+Na2CO3=CaCO3↓+2NaCl.
故答案为:(1)玻璃棒;
(2)取少量上层清液,滴加硫酸钠,若不产生白色沉淀,则证明氯化钡已经过量;
(3)BaCl2+Na2CO3=BaCO3↓+2NaCl,CaCl2+Na2CO3=CaCO3↓+2NaCl.
点评 本题考查了粗盐的提纯,是一道物质的提纯和分离的方法和操作的综合题,充分考查了学生的分析、解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.下列区分物质的方法中不正确的是( )
| A. | 熟石灰和烧碱:用水,观察是否放热 | |
| B. | 石灰水与氢氧化钠溶液:滴加酚酞溶液,看是否变色 | |
| C. | 黄金与黄铜(铜锌合金):滴加稀盐酸,观察是否有气泡产生 | |
| D. | 硫酸铜溶液和氯化铁溶液:用观察法 |
8.下列固体中不能用水鉴别的是( )
| A. | 熟石灰和生石灰 | B. | 硝酸铵和氯化钠 | C. | 硫酸铜和硫酸锌 | D. | 明矾和蔗糖 |
6.下列实验设计不合理的是( )
| A. | 用盐酸验证敞口放置的NaOH溶液已变质 | |
| B. | 用肥皂水区分氯化钙溶液和蒸馏水 | |
| C. | 用燃着木条区分氮气和二氧化碳 | |
| D. | 用碘酒区分淀粉和葡萄糖 |
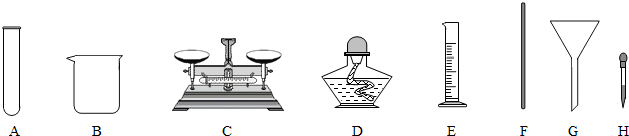 (1)配制时,在上面的仪器中除B、C、E外,还必须选用的是(填字母编号)FH.
(1)配制时,在上面的仪器中除B、C、E外,还必须选用的是(填字母编号)FH. 根据要求填空:
根据要求填空: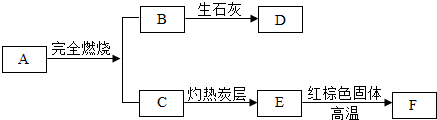 A~F是初中化学中的常见物质,如图是它们之间的转化关系,图中部分反应物或生成物未全部标出.已知:A是天然气的主要成分,B在常温下为液态,F是黑色粉末.
A~F是初中化学中的常见物质,如图是它们之间的转化关系,图中部分反应物或生成物未全部标出.已知:A是天然气的主要成分,B在常温下为液态,F是黑色粉末.