题目内容
10. 如图是密闭体系中某反应的微观示意图,“●”和“○”分别表示两种不同元素的原子,下列说法错误的是( )
如图是密闭体系中某反应的微观示意图,“●”和“○”分别表示两种不同元素的原子,下列说法错误的是( )| A. | 反应中,反应物分子发生了变化 | B. | 反应前后原子种类没有改变 | ||
| C. | 反应后该密闭体系中没有单质存在 | D. | 该反应是化合反应 |
分析 因为该反应的图示前后中存在相同的分子,所以说明反应过程中有部分分子没有参与反应,所以该图示可以转化为 ,据此对选项的内容逐一分析解答即可.
,据此对选项的内容逐一分析解答即可.
解答 解:因为该反应的图示前后中存在相同的分子,所以说明反应过程中有部分分子没有参与反应,所以该图示可以转化为 ;
;
A、由微粒的变化可知,反应中,反应物分子发生了变化,故A正确;
B、由微粒的变化可知,反应前后原子种类没有改变,故B正确;
C、反应后的生成物中没有同种原子构成的单质分子生成,在该密闭体系中部分不反应的单质分子还是存在的,故C错误;
D、由图示可知反应前物质中存在两种分子,而反应后为一种分子,所以该反应符合“多变一”的化合反应反应特征,故该反应属于化合反应,故D正确.
故选C.
点评 本题通过微观粒子的反应模型图,考查了微观上对化学反应的认识,学会通过微观示意图把宏观物质和微观粒子联系起来、从微观的角度分析物质的变化是正确解答此类题的关键.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
1.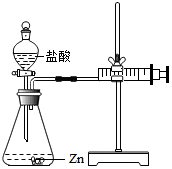 化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.
化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.
【提出问题】金属与盐酸反应的剧烈程度受哪些因素的影响?
【作出猜想】a.可能与金属本身的性质有关;
b.可能与盐酸的浓度有关.
【设计探究】实验所用金属均已用砂纸打磨
实验(1):为探究猜想a,小组同学分别在两支试管中放入相同质量的镁片和铁片,然后分别加入相同浓度和质量的稀盐酸,观察到放镁片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡,写出镁与稀盐酸发生反应的化学方程式Mg+2HCl=MgCl2+H2↑;从实验现象可判断:金属活动性Mg>Fe(填“<”“=”或“>”);
得出结论:金属与盐酸发生反应的剧烈程度与金属本身的性质有关,金属的活动性与反应的剧烈程度的关系是金属与盐酸反应的剧烈程度与金属本身性质有关(金属活动性越强,反应越剧烈).
实验(2):为探究猜想b,小组同学设计如图的装置进行实验,其中注射器的作用是通过注射器往右移动的体积判断生成氢气的体积所用药品、实验数据如表:
得出结论:金属与盐酸发生反应的剧烈程度与盐酸的浓度有关,其关系是其他条件相同时,盐酸浓度越大,反应越剧烈.
【反思评价】
(注意:若答对本小题将奖励4分,但化学试卷总分不超过60分)
根据表中实验II数据分析,请描述锌与盐酸发生反应快慢的变化情况并解释原因由慢到快然后逐渐减慢;锌与稀盐酸反应放热,随着反应的进行,温度升高,所以速度越来越快,一段时间后,盐酸被消耗,盐酸浓度变小,反应速率减慢.通过以上探究,你认为金属与盐酸反应的剧烈程度可能还受哪些因素的影响①温度;②金属表面积大小.(答两条即可)
 化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.
化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.【提出问题】金属与盐酸反应的剧烈程度受哪些因素的影响?
【作出猜想】a.可能与金属本身的性质有关;
b.可能与盐酸的浓度有关.
【设计探究】实验所用金属均已用砂纸打磨
实验(1):为探究猜想a,小组同学分别在两支试管中放入相同质量的镁片和铁片,然后分别加入相同浓度和质量的稀盐酸,观察到放镁片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡,写出镁与稀盐酸发生反应的化学方程式Mg+2HCl=MgCl2+H2↑;从实验现象可判断:金属活动性Mg>Fe(填“<”“=”或“>”);
得出结论:金属与盐酸发生反应的剧烈程度与金属本身的性质有关,金属的活动性与反应的剧烈程度的关系是金属与盐酸反应的剧烈程度与金属本身性质有关(金属活动性越强,反应越剧烈).
实验(2):为探究猜想b,小组同学设计如图的装置进行实验,其中注射器的作用是通过注射器往右移动的体积判断生成氢气的体积所用药品、实验数据如表:
| 实验 编号 | 选用金属 (均取2g) | 盐酸浓度 (均取50 mL) | 每30秒产生气体的体积/mL | |||||
| 30秒 | 30~ 60秒 | 60~ 90秒 | 90~ 120秒 | 120~ 150秒 | 前150秒收 集气体 | |||
| Ⅰ | 锌片 | 10% | 2.9 | 16.9 | 11.9 | 9.2 | 7.6 | 48.5 |
| Ⅱ | 锌片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
【反思评价】
(注意:若答对本小题将奖励4分,但化学试卷总分不超过60分)
根据表中实验II数据分析,请描述锌与盐酸发生反应快慢的变化情况并解释原因由慢到快然后逐渐减慢;锌与稀盐酸反应放热,随着反应的进行,温度升高,所以速度越来越快,一段时间后,盐酸被消耗,盐酸浓度变小,反应速率减慢.通过以上探究,你认为金属与盐酸反应的剧烈程度可能还受哪些因素的影响①温度;②金属表面积大小.(答两条即可)
18.学习化学要有分类的思想.下列物质属于纯净物的是( )
| A. | 海水 | B. | 冰水 | C. | 空气 | D. | 糖水 |
 在如图转化关系中,生成物D能使带星的木条复燃,F是一种常见的液体,H能使澄清石灰水变浑浊,在反应②中,B的质量和化学性质均没有改变.
在如图转化关系中,生成物D能使带星的木条复燃,F是一种常见的液体,H能使澄清石灰水变浑浊,在反应②中,B的质量和化学性质均没有改变.