题目内容
7.从C、H、O、S四种元素中选择符合要求的元素组成物质,将其化学符号填写在横线上.(1)相对分子质量最小的氧化物H2O;
(2)一种有毒且有刺激性气味的气体SO2;
(3)一种常温下为液体且常用于实验室制取氧气的物质H2O2.
分析 首先根据题意确定物质的化学名称,然后根据题目所提供的元素、书写化学式的方法和步骤写出物质的化学式即可.
解答 解:(1)氢元素是相对原子质量最小的元素,故其氧化物水是相对分子质量最小的氧化物,故填:H2O;
(2)由提供的元素组成的二氧化硫是一种有毒且有刺激性气味的气体,故填:SO2;
(3)过氧化氢是一种液体,在常温下常用来制取氧气,故填:H2O2
点评 本题难度不大,熟练掌握常见物质的性质、用途、组成及化学式的书写是正确解答此类题的关键所在;解题时应注意只能从给出的元素中选择来组成物质.

练习册系列答案
相关题目
4.五月初五,粽叶飘香,你能闻到香味是因为( )
| A. | 分子的质量小 | B. | 分子之间有间隙 | C. | 分子的体积小 | D. | 分子在不断运动 |
15.为了探究金属与酸反应的速率与哪些因素有关,小谷进行了以下实验探究:
【实验方案】
【发现问题】在同一反应中速率也不一样.
【继续探究】小谷对锌粉一稀硫酸反应过程中速率的变化情况进行探究.在100mL稀硫酸中加入足量的锌粉,用下图中的一种装置收集并测量氢气的体积.记录的实验数据如下表:
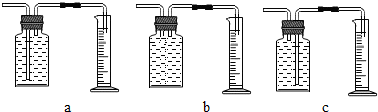
【讨论】(1)实验中测定反应产生氢气的体积可选用的装置是c(填序号),其中量筒的作用时根据进入量筒中水的体积,判断生成氢气的体积;
(2)实验数据反应,锌与稀硫酸反应的速率是先逐渐加快,一定时间后反应速率逐渐减慢,其原因是随着反应的进行,硫酸的浓度变小,反应速率变慢;
(3)若反应太剧烈,操作难以控制,为了减缓反应速率但又不减少产生氢气的质量,可在硫酸溶液中加入适量的(多选)AB.
A.蒸馏水 B.Na2SO4溶液 C.Na2CO3 D.CuO.
【实验方案】
| 实验步骤 | 现象 | 结论 |
| ①将足量铁粉与锌粉分别放入10%100mL稀硫酸中,观察现象 | 产生气泡速率:Fe<Zn | 反应速率与反应物的金属活动性强弱有关 |
| ②将等质量锌粉与锌片分别放入10%100mL稀硫酸中,观察现象 | 产生气泡速率:锌粉>锌片 | 反应速率与反应物的接触面积大小有关 |
【继续探究】小谷对锌粉一稀硫酸反应过程中速率的变化情况进行探究.在100mL稀硫酸中加入足量的锌粉,用下图中的一种装置收集并测量氢气的体积.记录的实验数据如下表:

| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
(2)实验数据反应,锌与稀硫酸反应的速率是先逐渐加快,一定时间后反应速率逐渐减慢,其原因是随着反应的进行,硫酸的浓度变小,反应速率变慢;
(3)若反应太剧烈,操作难以控制,为了减缓反应速率但又不减少产生氢气的质量,可在硫酸溶液中加入适量的(多选)AB.
A.蒸馏水 B.Na2SO4溶液 C.Na2CO3 D.CuO.
12.水是一种重要的自然资源,下列对水的认识正确的是( )
| A. | 自然界的水含量丰富,地球表面约71%被水覆盖,不存在水危机 | |
| B. | 经过沉淀、过滤、消毒后的水是一种纯净物 | |
| C. | 电解水实验可知,水中含有的氢气和氧气的体积比为2:1 | |
| D. | 硬水和软水指Ca2+、Mg2+含量不同的水,可用肥皂水加以搅拌进行区分 |
16.正确的设计实验方案时科学探究的重要环节.认真细致的观察和分析实验现象是获得化学知识的重要途径,以下化学实验设计能达到实验目的是( )
| A. | 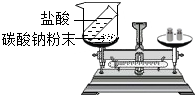 验证质量守恒定律 | B. | 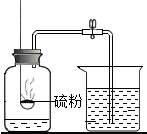 测定空气中的氧气含量 | ||
| C. |  证明CO2密度比空气大 | D. |  证明CO2能与水反应 |

 氧气的化学性质比较活泼,能支持燃烧,如图是木炭在氧气中燃烧实验室示意图,对该实验进行分析并回答.
氧气的化学性质比较活泼,能支持燃烧,如图是木炭在氧气中燃烧实验室示意图,对该实验进行分析并回答.