题目内容
物质的性质决定着物质在生产和生活中的用途.木炭和一氧化碳都具有还原性,可用于冶炼金属.请根据图回答:
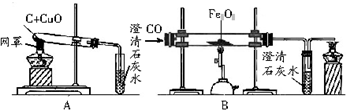
(1)A中的实验现象为: ;B中的实验现象为: ;
(2)请写出下列反应的化学方程式:①木炭还原氧化铜 ;②一氧化碳还原氧化铁 .(化学方程式2分)
(3)A、B装置中澄清石灰水的作用是 .
(4)B装置最右端酒精灯的作用是 .

(1)A中的实验现象为:
(2)请写出下列反应的化学方程式:①木炭还原氧化铜
(3)A、B装置中澄清石灰水的作用是
(4)B装置最右端酒精灯的作用是
考点:碳的化学性质,一氧化碳还原氧化铁,书写化学方程式、文字表达式、电离方程式
专题:碳单质与含碳化合物的性质与用途,金属与金属材料
分析:(1)根据碳、一氧化碳均具有还原性,碳与氧化铜反应生成铜和二氧化碳,一氧化碳与氧化铁反应生成铁和二氧化碳,进行分析解答.
(2)碳与氧化铜反应生成铜和二氧化碳,一氧化碳与氧化铁反应生成铁和二氧化碳写出反应的化学方程式即可.
(3)根据二氧化碳能使澄清的石灰水变浑浊,进行分析解答.
(4)根据一氧化碳有毒,直接排放到空气中会污染环境,可利用其具有可燃性,将尾气点燃转化为无毒的二氧化碳,进行分析解答.
(2)碳与氧化铜反应生成铜和二氧化碳,一氧化碳与氧化铁反应生成铁和二氧化碳写出反应的化学方程式即可.
(3)根据二氧化碳能使澄清的石灰水变浑浊,进行分析解答.
(4)根据一氧化碳有毒,直接排放到空气中会污染环境,可利用其具有可燃性,将尾气点燃转化为无毒的二氧化碳,进行分析解答.
解答:解:(1)碳、一氧化碳均具有还原性,碳与氧化铜反应生成铜和二氧化碳,一氧化碳与氧化铁反应生成铁和二氧化碳,A中会观察到黑色粉末变红,澄清的石灰水变浑浊;B中会观察到红色粉末变成黑色,澄清的石灰水变浑浊,
(2)碳与氧化铜反应生成铜和二氧化碳,一氧化碳与氧化铁反应生成铁和二氧化碳,反应的化学方程式分别是C+2CuO
2Cu+CO2↑、Fe2O3+3CO
2Fe+3CO2.
(3)二氧化碳能使澄清的石灰水变浑浊,A、B装置中澄清石灰水的作用是检验有无二氧化碳生成.
(4)一氧化碳有毒,直接排放到空气中会污染环境,B装置最右端酒精灯的作用是将尾气点燃,防止其污染空气.
故答案为:(1)黑色粉末变红,澄清的石灰水变浑浊;红色粉末变成黑色,澄清的石灰水变浑浊;(2)①C+2CuO
2Cu+CO2↑;②Fe2O3+3CO
2Fe+3CO2;(3)检验有无二氧化碳生成;(4)将尾气点燃,防止其污染空气.
(2)碳与氧化铜反应生成铜和二氧化碳,一氧化碳与氧化铁反应生成铁和二氧化碳,反应的化学方程式分别是C+2CuO
| ||
| ||
(3)二氧化碳能使澄清的石灰水变浑浊,A、B装置中澄清石灰水的作用是检验有无二氧化碳生成.
(4)一氧化碳有毒,直接排放到空气中会污染环境,B装置最右端酒精灯的作用是将尾气点燃,防止其污染空气.
故答案为:(1)黑色粉末变红,澄清的石灰水变浑浊;红色粉末变成黑色,澄清的石灰水变浑浊;(2)①C+2CuO
| ||
| ||
点评:本题难度不大,掌握碳还原氧化铜、一氧化碳还原氧化铁的实验原理、现象、化学方程式的书写等是正确解答本题的关键.

练习册系列答案
相关题目
下列行为不会造成空气污染的是( )
| A、整治农田时焚烧秸秆 |
| B、向蔬菜大棚中通入二氧化碳 |
| C、清理街道卫生时露天焚烧垃圾 |
| D、化工厂迁到城郊继续排放超标废气 |



 某课外活动小组在学习了书本“空气中氧气含量的测定”实验,知道P2O5不能随便排放在空气中,否则会对空气造成污染,所以对该实验进行了改进:
某课外活动小组在学习了书本“空气中氧气含量的测定”实验,知道P2O5不能随便排放在空气中,否则会对空气造成污染,所以对该实验进行了改进: