题目内容
(1)根据电解水实验装置图回答下列问题:
①C试管中为 气; C、D两试管中气体的质量比为 ;
②写出水在通电作用下反应的化学方程式
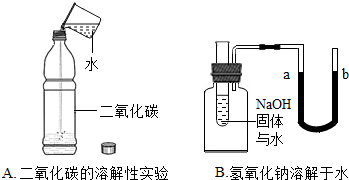
(2)小李和小高同学用一瓶久置的氢氧化钠溶液和稀硫酸做中和反应的实验,为了能够观察到明显现象,他们先向盛装l0mL氢氧化钠溶液的烧杯中滴加几滴酚酞试液,再逐滴滴加稀硫酸并不断搅拌.
①滴加稀硫酸的过程中观察到有气泡产生,他们发现氢氧化钠溶液已变质,请你写出
氢氧化钠溶液变质的化学方程式: .
②他们对该瓶氢氧化钠溶液的变质情况进行探究
【猜 想】猜想一:全部变质 猜想二:部分变质
【实验探究】他们按下列实验方案进行探究,请你帮他们把表补充完整:(温馨提示:氯化钡溶液呈中性)

①C试管中为
②写出水在通电作用下反应的化学方程式
(2)小李和小高同学用一瓶久置的氢氧化钠溶液和稀硫酸做中和反应的实验,为了能够观察到明显现象,他们先向盛装l0mL氢氧化钠溶液的烧杯中滴加几滴酚酞试液,再逐滴滴加稀硫酸并不断搅拌.
①滴加稀硫酸的过程中观察到有气泡产生,他们发现氢氧化钠溶液已变质,请你写出
氢氧化钠溶液变质的化学方程式:
②他们对该瓶氢氧化钠溶液的变质情况进行探究
【猜 想】猜想一:全部变质 猜想二:部分变质
【实验探究】他们按下列实验方案进行探究,请你帮他们把表补充完整:(温馨提示:氯化钡溶液呈中性)
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量上述氢氧化钠溶液于试管中,然后滴加过量氯化钡溶液,充分反应后过滤. | ① | 猜想二成立 |
| ②向所得溶液液中滴加几滴酚酞试液. | ② |
考点:电解水实验,碱的化学性质,中和反应及其应用,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:空气与水,科学探究
分析:(1)根据电解水产生的氢气体积大,氧气体积小,正极产生氧气,负极产生氢气,电解水获得的实验结论,要记住;
(2)运用二氧化碳和氢氧化钠反应生成碳酸钠和水解答.
【实验探究】①运用碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,氢氧化钠和氯化钡不反应解答.
②运用氯化钠的溶液呈中性不能使酚酞变红色、氢氧化钠的溶液呈碱性能使酚酞变红色解答.
(2)运用二氧化碳和氢氧化钠反应生成碳酸钠和水解答.
【实验探究】①运用碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,氢氧化钠和氯化钡不反应解答.
②运用氯化钠的溶液呈中性不能使酚酞变红色、氢氧化钠的溶液呈碱性能使酚酞变红色解答.
解答:解:(1)由正氧负氢,氢二氧一,可推出C试管产生的是氢气,D试管内气体是氧气,氢气和氧气的质量比为1:8;
(2)电解水时,正极产生的气体是氧气,负极产生的氢气是氢气,反应的化学方程式为2H2O
2H2↑+O2↑;
故答案为:(1)①氢;2:8;②2H2O
2H2↑+O2↑;
(2)二氧化碳和氢氧化钠反应生成碳酸钠和水,化学方程式:CO2+2NaOH=Na2CO3+H2O;故答案:CO2+2NaOH=Na2CO3+H2O.
【实验探究】①碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,但氢氧化钠不能和碳酸钡反应,故答案:产生白色沉淀;
②氯化钠的溶液呈中性不能使酚酞变红色、氢氧化钠的溶液呈碱性能使酚酞变红色,故答案:溶液由无色变为红色.
(2)电解水时,正极产生的气体是氧气,负极产生的氢气是氢气,反应的化学方程式为2H2O
| ||
故答案为:(1)①氢;2:8;②2H2O
| ||
(2)二氧化碳和氢氧化钠反应生成碳酸钠和水,化学方程式:CO2+2NaOH=Na2CO3+H2O;故答案:CO2+2NaOH=Na2CO3+H2O.
【实验探究】①碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,但氢氧化钠不能和碳酸钡反应,故答案:产生白色沉淀;
②氯化钠的溶液呈中性不能使酚酞变红色、氢氧化钠的溶液呈碱性能使酚酞变红色,故答案:溶液由无色变为红色.
点评:本题是科学探究题,主要考查酸碱盐的化学性质和复分解反应发生的条件;平时一定注意有特殊现象的化学反应,特别是产生沉淀的反应和沉淀的颜色要熟记要熟练掌握.

练习册系列答案
相关题目
下列实验基本操作中正确的是( )
| A、用滴管滴加液体时,滴管下端要紧贴试管内壁,防止液体溅出 |
| B、用镊子夹住块状药品,直接投入竖直的试管中 |
| C、向试管里倾倒液体时,试剂瓶口紧挨试管口 |
| D、实验结束后,剩余的试剂都应放回原试剂瓶 |