题目内容
12.回答下列问题: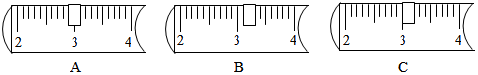
(1)实验室配制100g 10%的氯化钠溶液时,需要10g氯化钠固体.
(2)称量时如果用质量为23.1g的烧杯盛放固体,在托盘天平上已放30g的砝码,则天平上的游码位置应是右图的B(填字母).
(3)下列仪器中,量取水时需要用到c(填序号,下同)仪器和d仪器,溶解时需要用到a仪器和e仪器.
a.烧杯、b.10mL量筒、c.100mL量筒、d.滴管、e.玻璃棒、f.药匙、g.蒸发皿.
分析 (1)利用溶质质量=溶液质量×溶质的质量分数,进行分析解答.
(2)称量时如果用质量为23.1g的烧杯盛放固体,则烧杯和氯化钠的总质量为23.1g+10g=33.1g,进行分析解答.(3)根据溶剂质量=溶液质量-溶质质量,计算出所需水的质量和体积,进而判断所需量筒的量程,结合溶解操作所需的仪器,进行分析解答.
解答 解:(1)溶质质量=溶液质量×溶质的质量分数,配制100g 10%的氯化钠溶液,需氯化钠的质量=100g×10%=10g.
(2)称量时如果用质量为23.1g的烧杯盛放固体,则烧杯和氯化钠的总质量为23.1g+10g=33.1g,在托盘天平上已放30g的砝码,天平上的游码的质量应为33.1g-30g=3.1g,故天平上的游码位置应是右图的B.
(3)溶剂质量=溶液质量-溶质质量,所需溶剂的质量为100g-10g=90g(合90mL),应用规格为100mL的量筒量取水的体积;先用倾倒法加水到近刻度线,再改用胶头滴管加液到刻度线,用到的玻璃仪器是100mL量筒和胶头滴管.
溶解时需要用到烧杯和玻璃棒.
故答案为:(1)10;(2)B;(3)c;d;a;e.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤(计算、称量、溶解)、注意事项等是正确解答本题的关键.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
10.下列物质加入水中,可形成pH=10的溶液的是( )
| A. | HCl | B. | NaCl | C. | Na2CO3 | D. | KNO3 |
11.科学实验必须按规范进行操作,下列实验操作中规范的是( )
| A. |  读取液体体积 读取液体体积 | B. |  点燃酒精灯 点燃酒精灯 | ||
| C. |  检查装置的气密性 检查装置的气密性 | D. |  塞进橡皮塞 塞进橡皮塞 |
17.研究和学习化学,有许多重要的方法.下列方法中所举示例错误的是( )
| 选项 | 方法 | 示例 |
| A | 实验法 | 用磷做“测定空气中氧气含量”的实验 |
| B | 分类法 | 根据组成物质的元素种类,将纯净物分为单质和化合物 |
| C | 归纳法 | 根据稀盐酸、稀硫酸等物质的化学性质,归纳出酸的通性 |
| D | 类比法 | 根据金属铝能与稀盐酸反应,推测金属铜也能与稀盐酸反应 |
| A. | A | B. | B | C. | C | D. | D |
4.下列日常生活用品中,属于有机合成材料的是( )
| A. | 棉衬衣 | B. | 易拉罐 | C. | 尼龙绳 | D. | 玻璃杯 |
 如图是“×××”补钙剂商品标签图,根据标签信息完成下列问题
如图是“×××”补钙剂商品标签图,根据标签信息完成下列问题
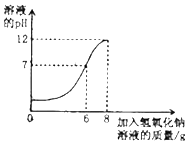 国家规定每100mL酿造食醋中含醋酸的质量标准为3.5~5.0g.某兴趣小组的同学对一市售食醋是否符合国家标准进行测定.他们取该食醋10mL,逐滴滴入5%的氢氧化钠溶液,记录数据,绘制成图.
国家规定每100mL酿造食醋中含醋酸的质量标准为3.5~5.0g.某兴趣小组的同学对一市售食醋是否符合国家标准进行测定.他们取该食醋10mL,逐滴滴入5%的氢氧化钠溶液,记录数据,绘制成图.