题目内容
2.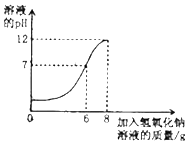 国家规定每100mL酿造食醋中含醋酸的质量标准为3.5~5.0g.某兴趣小组的同学对一市售食醋是否符合国家标准进行测定.他们取该食醋10mL,逐滴滴入5%的氢氧化钠溶液,记录数据,绘制成图.
国家规定每100mL酿造食醋中含醋酸的质量标准为3.5~5.0g.某兴趣小组的同学对一市售食醋是否符合国家标准进行测定.他们取该食醋10mL,逐滴滴入5%的氢氧化钠溶液,记录数据,绘制成图.(1)当加入氢氧化钠溶液为6g时,反应恰好完全.
(2)请计算这10mL市售食醋样品是否符合国家标准.(食醋和氢氧化钠反应的化学方程式:CH3COOH+NaOH═CH3COONa+H2O,假设该样品中其它物质不与氢氧化钠发生反应)
分析 (1)根据酸碱恰好完全反应时溶液的pH等于7分析回答;
(2)要知道该食醋是否符合国家标准,需要算出该食醋的总酸含量,与标准相比较,可利用醋酸与氢氧化钠反应的化学方程式,根据氢氧化钠的质量算出10ml食醋中含醋酸的质量,进而求出该食醋的总酸含量.
解答 解:(1)由图象可知,当加入6g的5%的氢氧化钠溶液是溶液的pH等于7,反应恰好完全.
(2)设10mL食醋样品中醋酸的质量为 x
CH3COOH+NaOH═CH3COONa+H2O
60 40
x 6g×5%
$\frac{60}{40}=\frac{x}{6g×5%}$ 解得:x=0.45g
则该食醋的总酸含量为4.5g/100ml.该食醋的总酸含量符合国家标准.
故答为:(1)6;(2)该食醋的总酸含量符合国家标准.
点评 本题主要考查了化学方程式计算的有关知识,同学们要准确掌握,难度不大.

练习册系列答案
相关题目
10.电能是电气时代不可或缺的二次能源,下列发电方式中利用了化学能源的是( )
| A. | 水力发电 | B. | 风力发电 | C. | 火力发电 | D. | 太阳能发电 |
17.下列应用及相应的原理(用化学方程式表示)都正确的是( )
| A. | 测定空气中氧气含量:4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | |
| B. | 用二氧化碳做碳酸饮料:CO2+H2O═H2CO3 | |
| C. | 实验室用过氧化氢溶液制取氧气:2H2O2═2H2O+O2↑ | |
| D. | 田径运动会上用红磷做发令枪的弹药:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 |
7.下列叙述与对应的示意图相符合的是( )
| A. |  将一瓶浓盐酸敞口露置在空气中 将一瓶浓盐酸敞口露置在空气中 | |
| B. |  向氯化钠和氯化钡的混合溶液中逐滴加入稀硫酸 向氯化钠和氯化钡的混合溶液中逐滴加入稀硫酸 | |
| C. | 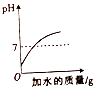 向醋酸中不断加入水 向醋酸中不断加入水 | |
| D. |  向质量和质量分数都相同的稀盐酸中不断加入铁片和镁条 向质量和质量分数都相同的稀盐酸中不断加入铁片和镁条 |
11.下列有关实验操作叙述正确的是( )
| A. | 为防止液体外洒,应将滴管伸入试管内 | |
| B. | 为了使配制的溶液浓度更准确,应在量筒内溶解溶质 | |
| C. | 稀释浓硫酸时,应将蒸馏水慢慢加到浓硫酸中并及时搅拌 | |
| D. | 用氢气还原氧化铜的实验结束时,先熄灭酒精灯,继续通H2直至生成物冷却 |
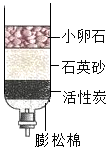 2010年到2012年,云南遭遇三年连旱,多地旱情严重,农作物受灾,目前干旱已造成云南超过310万人饮水困难.全省人民团结一致,共同抗旱,已见成效.
2010年到2012年,云南遭遇三年连旱,多地旱情严重,农作物受灾,目前干旱已造成云南超过310万人饮水困难.全省人民团结一致,共同抗旱,已见成效.