题目内容
3. 实验室里有一瓶标签残缺的试剂瓶,标签中只剩下“Na”和“10%”字样(如图所示),某兴趣小组对其组成进行如下探究.
实验室里有一瓶标签残缺的试剂瓶,标签中只剩下“Na”和“10%”字样(如图所示),某兴趣小组对其组成进行如下探究.【提出问题】这瓶试剂可能是什么溶液呢?
【查阅资料】
Ⅰ.初中化学中常见含钠的化合物有:NaCl、NaOH、Na2CO3、NaHCO3,其中一 种物质的类别有别于其它三种物质,该物质是氢氧化钠或NaOH.
Ⅱ.NaHCO3的水溶液呈碱性.
Ⅲ.室温(20℃)时,四种物质的溶解度数据如下:
| 物质 | NaHCO3 | NaCl | NaOH | Na2CO3 |
| 溶解度g/100g水 | 9.6 | 36 | 109 | 215 |
依据上述资料分析该瓶试剂不可能是碳酸氢钠的原因是20℃时饱和的碳酸氢钠溶液也达不到10%的浓度.
【实验探究】
实验1:
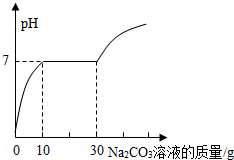
实验测得该溶液的pH>7,则这瓶试剂也不可能是氯化钠.
实验2:
为了检验该溶液是NaOH溶液还是Na2CO3溶液,又进行了如下实验:
取少量溶液于试管中,滴加足量的盐酸,有气泡产生,得出结论,该溶液是Na2CO3溶液.写出上述反应的化学方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑.
有同学对上述结论提出质疑,他认为该溶液可能由氢氧化钠和碳酸钠组成,并设计如下实验.
实验3:
另取样,加入过量的CaCl2溶液(呈中性),观察到有白色沉淀产生,设计这一步骤的目的是检验并除尽碳酸钠;静置后,取上层清液,滴入酚酞试液,溶液呈红色;得出结论,该同学的假设成立.
上述实验中,证明所加氯化钙溶液是过量的方法是取实验3中上层清液,滴加碳酸钠溶液,有白色沉淀产生,说明氯化钙是过量的.
分析 【查阅资料】根据物质的分类进行解答;
【资料分析】根据所给数据可以求出在20℃时各物质的饱和溶液的质量分数,可以做出判断;
【实验探究】实验2:根据盐酸和碳酸钠反应生成氯化钠、水和二氧化碳以及氢氧化钠溶液变质容易生成碳酸钠进行解答;
实验3:根据碳酸钠和氯化钙溶液反应生成碳酸钙沉淀和氯化钠,氢氧化钠溶液呈碱性,能使酚酞试液变红进行解答.
解答 解:【查阅资料】氢氧化钠属于碱,而氯化钠、碳酸钠、碳酸氢钠属于盐;
【资料分析】根据计算可以知道在20℃时饱和碳酸氢钠的质量分数为:$\frac{9.6g}{100g+9.6g}$×100%=8.8%,而题目中标注的溶液的质量分数为10%,所以能够排除碳酸氢钠;
【实验探究】实验2:
盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,所以取少量溶液于试管中,滴加足量的盐酸,有气泡产生,得出结论,该溶液是Na2CO3溶液.上述反应的化学方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
氢氧化钠溶液变质容易生成碳酸钠,所以该溶液可能由氢氧化钠和碳酸钠组成;
实验3:碳酸钠和氯化钙溶液反应生成碳酸钙沉淀和氯化钠,所以另取样,加入过量的CaCl2溶液(呈中性),观察到有白色沉淀产生,设计这一步骤的目的是检验并除尽碳酸钠;氢氧化钠溶液呈碱性,能使酚酞试液变红,静置后,取上层清液,滴入酚酞试液,溶液呈红色,所以含有氢氧化钠;上述实验中,证明所加氯化钙溶液是过量的方法是:取实验3中上层清液,滴加碳酸钠溶液,有白色沉淀产生,说明氯化钙是过量的.
故答案为:
【查阅资料】氢氧化钠或NaOH;
【资料分析】20℃时饱和的碳酸氢钠溶液也达不到10%的浓度;
【实验探究】实验2:Na2CO3+2HCl=2NaCl+H2O+CO2↑;氢氧化钠和碳酸钠;
实验3:检验并除尽碳酸钠;
取实验3中上层清液,滴加碳酸钠溶液,有白色沉淀产生,说明氯化钙是过量的.
点评 本题考查了破损标签试剂的确定,完成此题,可以依据破损标签的部分已经有关物质的性质进行.要求同学们熟练掌握有关物质的性质,以便灵活应用.

 阅读快车系列答案
阅读快车系列答案| A. | 活性炭作净水剂 | |
| B. | 无水硫酸铜用于检验酒精中是否含水 | |
| C. | 熟石灰可治疗胃酸过多 | |
| D. | 稀有气体制成多种用途的电光源 |
| 氯化钡溶液 | 氧化铜粉末 | 氢氧化钠溶液 | |
| 物质X | 白色沉淀 | 溶解,溶液变蓝 | 无明显现象 |
| A. | 硫酸钠溶液 | B. | 稀硫酸 | C. | 稀硝酸 | D. | 澄清的石灰水 |
 某化学兴趣小组的同学进行了以下实验:向烧杯中加入变质的氢氧化钙固体和一定量的稀盐酸,一段时间后固体全溶解.他们对所得溶液中的溶质成分进行了探究.
某化学兴趣小组的同学进行了以下实验:向烧杯中加入变质的氢氧化钙固体和一定量的稀盐酸,一段时间后固体全溶解.他们对所得溶液中的溶质成分进行了探究.