题目内容
18.某化学兴趣小组的同学对实验室里的粗盐样品进行了如下实验探究如图1: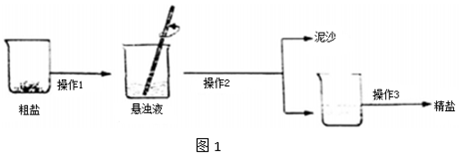
(1)操作②的名称过滤.
(2)操作③中玻璃棒的作用搅拌,防止因局部温度过高,造成液滴飞溅.
兴趣小组的同学查阅资料得知:
①精盐中还含有少量的可溶性杂质(假定可溶性杂质只有氯化镁一种).
②MgCl2+2NaOH═Mg(OH)2↓+2NaCl.
为了得到纯净的氯化钠,兴趣小组将所得到的精盐又作了如下解释如图2.
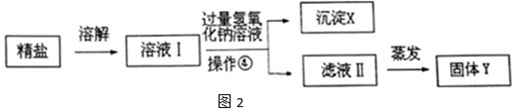
(3)写出沉淀X的化学式Mg(OH)2.
(4)加入过量氢氧化钠溶液目的是除尽杂质氯化镁.
(5)兴趣小组同学在实验过程中,又发现了新的问题:此方案很容易引入新的杂质,请写出固体物质Y的成分NaCl、NaOH(用化学式表示).
(6)兴趣小组同学继续探究后又提出新的方案:向滤液Ⅱ中滴加过量盐酸既能除去NaOH杂质,又能有效地防止新杂质的引入,写出有关反应的化学方程式:NaOH+HCl=NaCl+H2O.
分析 (1)根据过滤可以将不溶性固体从溶液中分离进行分析;
(2)根据操作③是蒸发,玻璃棒的作用是:搅拌,防止因局部温度过高,造成液滴飞溅进行分析;
(3)根据氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠进行分析;
(4)根据氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠进行分析;
(5)根据在除杂过程中加入的氢氧化钠是过量的进行分析;
(6)根据盐酸和氢氧化钠反应生成氯化钠和水进行分析.
解答 解:(1)过滤可以将不溶性固体从溶液中分离,所以操作②的名称是过滤;
(2)操作③是蒸发,玻璃棒的作用是:搅拌,防止因局部温度过高,造成液滴飞溅;
(3)氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,所以沉淀X的化学式是:Mg(OH)2;
(4)氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,所以加入过量氢氧化钠溶液目的是除尽杂质氯化镁;
(5)在除杂过程中加入的氢氧化钠是过量的,所以固体物质Y的成分是:NaCl、NaOH;
(6)盐酸和氢氧化钠反应生成氯化钠和水,化学方程式为:NaOH+HCl=NaCl+H2O.
故答案为:(1)过滤;
(2)搅拌,防止因局部温度过高,造成液滴飞溅;
(3)Mg(OH)2;
(4)除尽杂质氯化镁;
(5)NaCl、NaOH;
(6)NaOH+HCl=NaCl+H2O.
点评 在解此类题时,首先要知道除去的杂质的离子的性质,然后选择合适的试剂和滴加顺序进行除杂,一般加碳酸根离子要放在加钡离子之后,可以将剩余的钡离子除去,除杂的结果,最后只能有先氯化钠,也就是氯离子和钠离子.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
9.实验室里取8mL水并进行加热,下列需用的化学仪器组合正确的是( )
①带铁夹的铁架台 ②10mL量筒 ③100mL量筒 ④酒精灯 ⑤石棉网 ⑥试管 ⑦试管夹 ⑧胶头滴管.
①带铁夹的铁架台 ②10mL量筒 ③100mL量筒 ④酒精灯 ⑤石棉网 ⑥试管 ⑦试管夹 ⑧胶头滴管.
| A. | ②④⑥⑦⑧ | B. | ①③④⑥⑧ | C. | ①②④⑥ | D. | ①②④⑤⑥ |
6.下列化学用语中,对“2”的含义表述不正确的是( )
| A. | 2H--2个氢原子 | B. | H2--1个氢分子中含有2个氢原子 | ||
| C. | 2NH3-2个氨分子 | D. | S2---硫元素的化合价为-2 |
10.近年来我区陆续建立了许多生态农庄,为广大市民假日游玩提供了新的去处,赏花、观景、摘草莓等极大丰富了市民的假日生活.下列有关说法正确的是( )
| A. | 为了增加草莓产量,可以大量使用化肥农药 | |
| B. | 就地焚烧农庄中的秸秆可以增加田地肥效 | |
| C. | 方便生活,推广使用一次性塑料餐盒 | |
| D. | 绿色出行,提倡乘坐公共交通工具 |
7.下列有关实验,所用的主要仪器合理的是( )
| 项目 | 实验名称 | 主要仪器 |
| A | 蒸发食盐水得到食盐 | 酒精灯、烧杯、玻璃棒 |
| B | 实验室制取氧气结束后,利用过滤法回收二氧化锰 | 烧杯、普通漏斗 |
| C | 研磨硫酸铵与熟石灰的混合物检验铵态氮肥 | 研钵、研杵 |
| D | 用氯化钠配制一定质量分数的氯化钠溶液 | 托盘天平、烧杯、玻璃棒 |
| A. | A | B. | B | C. | C | D. | D |
8.里约奥运奖牌的制作过程有以下几个重要步骤,其中主要涉及化学变化的是( )
| A. | 手工制作金属模具 | B. | 模具扫描输入电脑制作 | ||
| C. | 显微镜下仔细检查 | D. | 铸造厂电镀合成 |