题目内容
19.(1)只用Na、O、Cl、H四种元素中的一种或几种,按要求各写一个化学式:酸HCl; 碱NaOH;(2)请用化学方程式解释下列现象或做法:
①人的胃液中含有少量盐酸,服用少量细铁粉,能治疗缺铁性贫血Fe+2HCl=FeCl2+H2↑
②食品包装袋中的干燥剂(主要成分是氧化钙)有防潮作用CaO+H2O=Ca(OH)2
③用稀盐酸除铁锈Fe2O3+6HCl=2FeCl3+3H2O
④长期存放的氢氧化钠溶液,因保存不当而发生变质CO2+2NaOH=Na2CO3+H2O.
分析 (1)本题利用H、O、Na、Cl四种元素来书写常见物质的化学式,然后根据酸、碱的概念来解答;
(2)只有熟悉反应物、生成物和反应条件,依据质量守恒定律的两个原则,才能写出正确的化学方程式.
解答 解:(1)电离时生成的阳离子都是氢离子的化合物是酸,由提供的元素组成的HCl属于酸;故填:HCl;
电离时生成的阴离子都是氢氧根离子的化合物是碱,由提供的元素组成的NaOH属于碱;故填:NaOH;
(2)①胃液中含有盐酸,能与铁反应生成氯化亚铁和氢气,可用于补铁;故填:Fe+2HCl=FeCl2+H2↑;
②氧化钙能与水反应生成氢氧化钙;故填:CaO+H2O=Ca(OH)2;
③铁锈的主要成分是氧化铁,氧化铁与稀盐酸反应生成氯化铁和水;故填:Fe2O3+6HCl=2FeCl3+3H2O;
④空气中的二氧化碳与氢氧化钠反应生成碳酸钠和水,故填:CO2+2NaOH=Na2CO3+H2O.
点评 本题要求学生会正确书写化学方程式,并会把化学方程式的书写和生产、生活和科研中的一些常识结合起来,灵活运用.

练习册系列答案
相关题目
7.下列图象能正确反映对应变化关系的是( )
| 序号 | 实验内容 | x轴含义 | y轴含义 | 坐标图 |
| ① | 向一定量铁粉和铜粉中不断滴加硫酸铜溶液 | 硫酸铜溶液质量 | 单质铜的质量 |  |
| ② | 向氢氧化钠溶液中逐滴加入稀盐酸 | 稀盐酸质量 | 所得溶液中水的质量 | |
| ③ | 一定温度下,向某不饱和氯化钠溶液中加入氯化钠固体 | 加入氯化钠质量 | 溶液中溶质的质量分数 | |
| ④ | 加热高锰酸钾制取氧气 | 加热时间 | 剩余固体 |
| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
14.下列说法错误的是( )
| A. | 分离液态空气法制氧气属于分解反应 | |
| B. | 电解水生成氢气和氧气,说明水是由氢、氧两种元素组成的 | |
| C. | 自然界的水多数是混合物,通过蒸馏方法可得到纯净物 | |
| D. | 打开盛浓盐酸的瓶盖,可观察到瓶口有白雾出现 |
4.对有关实验现象的描述正确的是( )
| A. | 红磷点燃后伸入充空气的集气瓶中,产生大量白烟 | |
| B. | 将铁丝伸入充满氧气的集气瓶中,剧烈燃烧,生成氧化铁 | |
| C. | 硫粉在氧气中燃烧产生微弱的淡蓝色火焰 | |
| D. | 木炭燃烧生成二氧化碳 |
11.某班同学用氢氧化钠溶液和稀盐酸进行中和反应实验.
(1)甲同学实验操作如图甲.
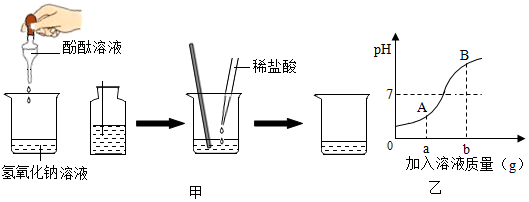
在烧杯中加入约5mL氢氧化钠溶液,滴入几滴无色酚酞溶液,此时溶液呈红色.使用胶头滴管吸取液体时,要先按着橡胶帽排干净空气,再放入滴瓶中吸取液体.
接着用滴管滴入一定量的稀盐酸,再用玻璃棒搅拌,发现溶液为无色,于是甲同学得出两者恰好中和的结论,反应的化学方程式为NaOH+HCl═NaCl+H2O.
(2)乙同学对甲同学的结论提出了质疑,并对反应后溶液中的溶质成分进行探究.
【实验探究】
反应后溶液中的溶质是什么?
猜想一:只有NaCl. 猜想二:NaCl和HCl.猜想三:NaCl和NaOH.
以上猜想中,你觉得不合理的是猜想三.
为了验证另外两种猜想,乙同学设计如下实验方案:
(3)图乙是稀HCl和NaOH溶液反应的pH变化曲线,以下说法正确的是CD(多选)
A.该反应是稀HCl滴入NaOH溶液中
B.ag是指加入氢氧化钠固体质量
C.A点溶液的溶质为HCl和NaCl
D.检验B点溶液的溶质先滴加足量的Mg(NO3)2,静置后再滴入少量AgNO3.
(1)甲同学实验操作如图甲.

在烧杯中加入约5mL氢氧化钠溶液,滴入几滴无色酚酞溶液,此时溶液呈红色.使用胶头滴管吸取液体时,要先按着橡胶帽排干净空气,再放入滴瓶中吸取液体.
接着用滴管滴入一定量的稀盐酸,再用玻璃棒搅拌,发现溶液为无色,于是甲同学得出两者恰好中和的结论,反应的化学方程式为NaOH+HCl═NaCl+H2O.
(2)乙同学对甲同学的结论提出了质疑,并对反应后溶液中的溶质成分进行探究.
【实验探究】
反应后溶液中的溶质是什么?
猜想一:只有NaCl. 猜想二:NaCl和HCl.猜想三:NaCl和NaOH.
以上猜想中,你觉得不合理的是猜想三.
为了验证另外两种猜想,乙同学设计如下实验方案:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量反应后的溶液于试管中滴入Na2CO3溶液 | 产生气泡 | 猜想二成立 |
| 取少量反应后的溶液于试管中加入锌粒 | 没有气泡产生 | 猜想一成立 |
A.该反应是稀HCl滴入NaOH溶液中
B.ag是指加入氢氧化钠固体质量
C.A点溶液的溶质为HCl和NaCl
D.检验B点溶液的溶质先滴加足量的Mg(NO3)2,静置后再滴入少量AgNO3.
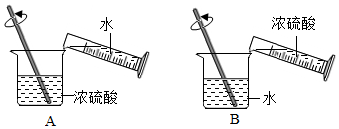
 九年级某班的化学兴趣小组对“氢氧化钠与稀盐酸的中和反应”进行了实验探究.
九年级某班的化学兴趣小组对“氢氧化钠与稀盐酸的中和反应”进行了实验探究.