题目内容
3.某同学设计了如图A-F气体制取与性质的组合装置,打开活塞K,很快看到F装置中蜡烛由下至上依次熄灭.请根据如图回答问题.
(1)仪器①的名称为:长颈漏斗.
(2)小华用G装置加热高锰酸钾制取氧气时,发现试管位置过高,他调节试管过度需要操作的旋钮是③.
(3)利用A装置制取气体的优点:可使反应随时发生或停止;A装置中发生的化学反应方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(4)B装置中观察到的现象为导管口有气泡冒出,白磷燃烧.
(5)D装置中发生的化学反应方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.
(6)E装置中观察到石蕊试液变红,用化学方程式解释产生该现象的原因CO2+H2O=H2CO3.
(7)F装置中蜡烛熄灭的原因是二氧化碳不燃烧、也不支持燃烧,密度比空气大.
分析 (1)根据仪器名称分析;
(2)根据装置特点来分析;
(3)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气,据此写出反应的方程式;
(4)根据燃烧条件来分析;
(5)根据稀盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,进行分析解答
(6)根据显酸性的溶液能使石蕊试液变红色分析;
(7)根据二氧化碳的性质来分析;
解答 解:(1)仪器①为长颈漏斗;故填:长颈漏斗;
(2)由图示可知,调节试管过度需要操作的旋钮是③;故填:③;
(3)A装置可使反应随时发生或停止,节约样品;A中的反应是过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;故填:可使反应随时发生或停止;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(4)B装置中观察到的现象为导管口有气泡冒出,白磷燃烧;故填:导管口有气泡冒出,白磷燃烧;
(5)稀盐酸与石灰石反应制取二氧化碳,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳.故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(6)E中导管口有气泡冒出,说明二氧化碳进入石蕊试液中,二氧化碳能和石蕊试液中的水反应生成碳酸,碳酸显酸性,能使石蕊试液变红色,因此溶液由紫色变为红色;故填:CO2+H2O=H2CO3;
(7)F装置中蜡烛熄灭的原因是二氧化碳不燃烧、也不支持燃烧,密度比空气大;故填:二氧化碳不燃烧、也不支持燃烧,密度比空气大;
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
11.下列实验基本操作正确的是( )
| A. |  称量NaCl固体 | B. |  稀释浓硫酸 | C. |  蒸发食盐水 | D. |  滴加液体 |
18.在“宏观-微观-符号”之间建立联系,是化学学科特有的思维方式,如图是某反应的微观示意图,下列说法正确的是( )
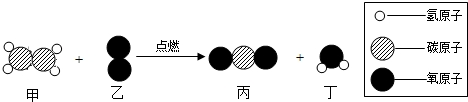

| A. | 该反应中有四种化合物 | |
| B. | 参加反应的甲、乙分子个数比为1:3 | |
| C. | 该反应属于置换反应 | |
| D. | 参加反应的甲、乙物质的质量比为28:32 |
7.下列过程中发生的能量变化属于化学能转化为电能的是( )
| A. | 天然气燃烧 | B. | 电解水制氢气 | C. | 核能发电 | D. | 干电池放电 |


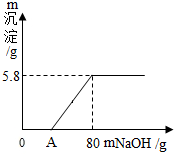 向100g稀H2SO4溶液中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入质量分数为20%的NaOH溶液,所得沉淀质量与加入NaOH溶液质量关系如图所示.请回答:
向100g稀H2SO4溶液中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入质量分数为20%的NaOH溶液,所得沉淀质量与加入NaOH溶液质量关系如图所示.请回答: