题目内容
4.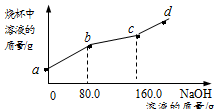 烧杯中盛有CuSO4和H2SO4的混合溶液100g,向其中滴加10%的NaOH溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示,下列说法正确的是( )
烧杯中盛有CuSO4和H2SO4的混合溶液100g,向其中滴加10%的NaOH溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示,下列说法正确的是( )| A. | ab段反应产生蓝色沉淀 | B. | bc段溶液增加70.2g | ||
| C. | c点对应的溶液质量为260g | D. | d点溶液中的溶质只有氢氧化钠 |
分析 向盛有CuSO4和H2SO4的混合溶液100g中滴加10%的NaOH溶液,氢氧化钠首先与稀硫酸反应生成了硫酸钠和水,当稀硫酸反应完后,再与硫酸铜反应生成了氢氧化铜沉淀和硫酸钠,据此分析判断有关的说法.
解答 解:由题意可知,向盛有CuSO4和H2SO4的混合溶液100g中滴加10%的NaOH溶液,氢氧化钠首先与稀硫酸反应生成了硫酸钠和水,当稀硫酸反应完后,再与硫酸铜反应生成了氢氧化铜沉淀和硫酸钠.
A、由图象可知,ab段反应是氢氧化钠与稀硫酸反应生成了硫酸钠和水,故A说法错误;
B、由题意可是:与硫酸铜反应的氢氧化钠的质量为:(160.0g-80.0g)×10%=8g,
设生成的氢氧化铜的质量为x、生成的硫酸钠的质量为y,
2NaOH+CuSO4=Na2SO4+Cu(OH)2↓;
80 142 98
8g y x
$\frac{80}{98}$=$\frac{8g}{x}$,x=9.8g
$\frac{80}{142}$=$\frac{8g}{y}$,y=14.2g
bc段溶液增加的溶液的质量是80g-9.8g=70.2g
由以上计算可知,B说法正确;
C、c点对应的溶液质量为100g+160g-9.8g≠260g,故错误.
D、d点溶液中有生成的硫酸钠、过量的氢氧化钠,故说法错误.
故选B.
点评 本题的综合性较强,难度较大,熟练掌握酸、碱、盐的性质和根据根据化学方程式的计算是解答本题基础知识.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案
相关题目
15. “中国高铁”已是国家的新外交名片,高铁车身主要是用镍铬奥氏体不锈钢制成的,如图为铬元素在元素周期表中的信息,下列说法正确的是( )
“中国高铁”已是国家的新外交名片,高铁车身主要是用镍铬奥氏体不锈钢制成的,如图为铬元素在元素周期表中的信息,下列说法正确的是( )
 “中国高铁”已是国家的新外交名片,高铁车身主要是用镍铬奥氏体不锈钢制成的,如图为铬元素在元素周期表中的信息,下列说法正确的是( )
“中国高铁”已是国家的新外交名片,高铁车身主要是用镍铬奥氏体不锈钢制成的,如图为铬元素在元素周期表中的信息,下列说法正确的是( )| A. | 铬元素属于非金属元素 | B. | 铬原子的质子数为52 | ||
| C. | 铬元素的原子序数为24 | D. | 铬元素在地壳中的含量为52.0% |
12.下列属于化学变化的是( )
| A. | 盐酸挥发 | B. | 铁生锈 | C. | 冰融化 | D. | 过滤 |
19.下列指定反应的化学方程式正确的是( )
| A. | 铁丝在氧气中燃烧:4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | |
| B. | 古代湿法炼铜:Fe+CuSO4═FeSO4+Cu | |
| C. | 用盐酸除铁锈:FeO+2HC1═FeC12+H2O | |
| D. | 用氢氧化钠溶液吸收二氧化硫:SO2+2NaOH═Na2SO4+H2O |
16.氧气是我们身边常见的物质,以下有关氧气的叙述正确的是( )
| A. | 凉开水不能用养鱼,说明凉开水中不含氧元素 | |
| B. | 钢铁生锈是有氧气参加的缓慢氧化 | |
| C. | 细铁丝在氧气中剧烈燃烧,火星四射,生成黑色的氧化铁固体 | |
| D. | 物质和氧气的反应都属于化合反应 |
13.在我国的南方,每年春节,家家户户都要吃汤圆.汤圆是由糯米和汤圆心子组成,其中汤圆心子的主要原料是蔗糖,蔗糖的化学式为C12H22O11,下列说法正确的是( )
| A. | 每个蔗糖分子含有45个原子 | B. | 汤圆心子和蔗糖都是混合物 | ||
| C. | 蔗糖中氢、氧两元素的质量比为2:1 | D. | 蔗糖的相对分子质量为144 |
 ,且0<y≤8.请回答下列问题:
,且0<y≤8.请回答下列问题: