题目内容
9.请结合图示实验装置,回答下列问题.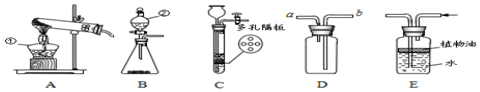
(1)写出有标号的仪器名称:②分液漏斗.
(2)用高锰酸钾制氧气选用的发生装置是A(选填序号),化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)若用石灰石和稀盐酸制取二氧化碳,该反应化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,
再用D装置收集,气体应从b端通入(选填“a”或“b”).
(4)实验室可用B或C装置制H2,反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑,C相对于B装置的优点有可以控制反应的发生和停止.
(5)若用E装置收集HCl气体,需在水上放一层植物油,由此推测HCl气体可能具有的物理性质是能溶于水或与水反应.
分析 分液漏斗可以控制反应的速率,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集.若用E装置收集HCl气体,需在水上放一层植物油,由此推测HCl气体可能具有的物理性质是:能溶于水或与水反应.
解答 解:(1)分液漏斗可以控制反应的速率,故答案为:分液漏斗;
(2)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;故答案为:A;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;再用D装置收集,气体应从长管进入,因为二氧化碳的密度比空气密度大,故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;b;
(4)实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集;C相对于B装置的优点有:可以控制反应的发生和停止;故答案为:Zn+H2SO4=ZnSO4+H2↑;可以控制反应的发生和停止;
(5)若用E装置收集HCl气体,需在水上放一层植物油,由此推测HCl气体可能具有的物理性质是:能溶于水或与水反应;故答案为:能溶于水或与水反应;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、注意事项和气体的性质等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案| 选项 | 鉴别的物质 | 鉴别的方法 |
| A | 冰和干冰 | 室温(20℃)放置,过一段观察是否有痕渍 |
| B | 水和双氧水 | 加二氧化锰,观察是否有气泡 |
| C | 纯羊毛和化纤面料 | 灼烧闻气味 |
| D | 二氧化锰和氧化铜 | 观察颜色 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 利用金属的年代: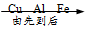 | B. | 硫元素的化合价: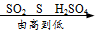 | C. | 物质的溶解性: | D. | 含碳量的高低: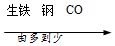 |
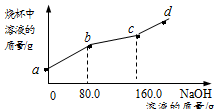 烧杯中盛有CuSO4和H2SO4的混合溶液100g,向其中滴加10%的NaOH溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示,下列说法正确的是( )
烧杯中盛有CuSO4和H2SO4的混合溶液100g,向其中滴加10%的NaOH溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示,下列说法正确的是( )| A. | ab段反应产生蓝色沉淀 | B. | bc段溶液增加70.2g | ||
| C. | c点对应的溶液质量为260g | D. | d点溶液中的溶质只有氢氧化钠 |
| A. | 用食盐水消毒杀菌 | B. | 用霉变花生榨花生油 | ||
| C. | 用甲醛溶液保存海鲜 | D. | 用含亚硝酸钠的工业用盐烹调食物 |
 如图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是C
如图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是C