题目内容
15.关于“K2CO3”说法错误的是( )| A. | 名称:碳酸钾 | B. | 类别:盐 | C. | 焰色反应:黄色 | D. | 用途:可作钾肥 |
分析 “K2CO3”是碳酸钾的化学式,属于盐,是白色固体,可以用作钾肥.
解答 解:A、K2CO3的名称是碳酸钾,该选项说法正确;
B、碳酸钾是由钾离子和碳酸根离子组成的化合物,属于盐,该选项说法正确;
C、钾离子的焰色反应是紫色,该选项说法不正确;
D、碳酸钾中含有钾元素,可以用作钾肥,该选项说法正确.
故选:C.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
5.甲、乙、丙、丁四种物质的转化关系如图所示.下列说法正确的是( )


| A. | 若丙为气体,则甲、乙中一定有单质 | |
| B. | 若丙为沉淀,则甲、乙中一定有一种物质是碱 | |
| C. | 若丁为水,则该反应不一定是中和反应 | |
| D. | 若甲、乙、丙、丁为化合物,则该反应一定是复分解反应 |
6.除去下列物质中的少量杂质,所用方法正确的是( )
| 选项 | 物质(括号内为杂质) | 除杂方法 |
| A | NaCl(Na2CO3) | 加入适量的稀盐酸,蒸发、结晶 |
| B | KCl(MnO2) | 加水溶解、过滤、洗涤、干燥 |
| C | CO2(CO) | 通过灼热的氧化铜 |
| D | CaO(CaCO3) | 加入适量的稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |
10.如图是一定量的铝与氧化铜的混合物在高温时发生化学反应的微观示意图,下列说法中正确的是( )

| A. | 反应前后各元素的化合价都保持不变 | |
| B. | 化学反应中共有三种生成物 | |
| C. | 反应前后共有两种氧化物 | |
| D. | 参加反应的铝与氧化铜的化学计量数之比为4:3 |
14.锌及其氧化物(ZnO,白色,难溶于水,溶于强酸)具有广泛的应用.
(一)锌的广泛应用
(1)锌被称之为“生命元素”.儿童、青少年如果缺锌严重,将会导致食欲不振和智力发育不良.经常吃贝壳类海产品、红色肉类等含锌的食物有利补“锌”.这里的“锌”是指B.
A.单质 B.元素 C.原子 D.分子
(2)锌与铜熔合可形成“黄铜”,它属于A(选填序号).
A.金属材料 B.无机非金属材料 C.合成材料 D.复合材料
(二)活性ZnO制取的探究
【实验方案】工业上用粗氧化锌(含少量FeO)制取活性氧化锌,其流程如下:
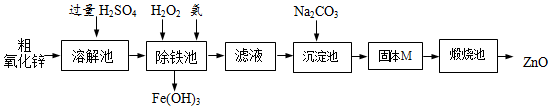
【查阅资料】一些阳离子以氢氧化物形式开始沉淀、完全沉淀时溶液的pH见表.
【问题探究】
(3)“溶解”前将粗氧化锌粉碎成细颗粒,目的是增大接触面积,加快反应速率.
(4)写出在粗ZnO样品中加硫酸发生反应的化学方程式ZnO+H2SO4═ZnSO4+H2O(选写一个).
(5)“溶解”后得到的酸性溶液中含有ZnSO4、H2SO4、FeSO4.除铁池中加入适量H2O2,使Fe2+转化为Fe3+;为使溶液中Fe3+全部转化为Fe(OH)3,而Zn2+不形成Zn(OH)2,则应加入氨水控制溶液的pH的范围为3.2~6.2.
【组成测定】固体B的组成会影响制得的ZnO的活性.为确定aZnCO3•bZn(OH)2•cH2O的组成,进行如下实验(假设每步反应、吸收均完全):
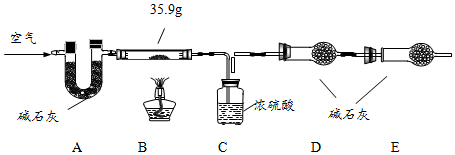
【查阅资料】aZnCO3•bZn(OH)2•cH2O受热分解生成ZnO、H2O、CO2三种产物.
(6)写出装置B中发生反应的化学方程式aZnCO3•bZn(OH)2•cH2O$\frac{\underline{\;\;△\;\;}}{\;}$(a+b)ZnO+aCO2↑+(b+c)H2O .
现称取35.9g aZnCO3•bZn(OH)2•cH2O在B装置中进行完全煅烧,测得装置C和D的质量分别增重7.2g和4.4g.
【实验分析及数据处理】
(7)装置A的作用是除去空气中二氧化碳和水.
(8)根据上述数据,则生成ZnO的质量为24.3 g;a:b:c=1:2:2.
(9)若没有E装置,则测得的a值偏大(填“偏大”、“偏小”或“不变”).
(一)锌的广泛应用
(1)锌被称之为“生命元素”.儿童、青少年如果缺锌严重,将会导致食欲不振和智力发育不良.经常吃贝壳类海产品、红色肉类等含锌的食物有利补“锌”.这里的“锌”是指B.
A.单质 B.元素 C.原子 D.分子
(2)锌与铜熔合可形成“黄铜”,它属于A(选填序号).
A.金属材料 B.无机非金属材料 C.合成材料 D.复合材料
(二)活性ZnO制取的探究
【实验方案】工业上用粗氧化锌(含少量FeO)制取活性氧化锌,其流程如下:

【查阅资料】一些阳离子以氢氧化物形式开始沉淀、完全沉淀时溶液的pH见表.
| 沉淀物 | Fe(OH)3 | Zn(OH)2 | Fe(OH)2 |
| 开始沉淀pH | 1.5 | 6.2 | 6.3 |
| 完全沉淀pH | 3.2 | 8.0 | 9.7 |
(3)“溶解”前将粗氧化锌粉碎成细颗粒,目的是增大接触面积,加快反应速率.
(4)写出在粗ZnO样品中加硫酸发生反应的化学方程式ZnO+H2SO4═ZnSO4+H2O(选写一个).
(5)“溶解”后得到的酸性溶液中含有ZnSO4、H2SO4、FeSO4.除铁池中加入适量H2O2,使Fe2+转化为Fe3+;为使溶液中Fe3+全部转化为Fe(OH)3,而Zn2+不形成Zn(OH)2,则应加入氨水控制溶液的pH的范围为3.2~6.2.
【组成测定】固体B的组成会影响制得的ZnO的活性.为确定aZnCO3•bZn(OH)2•cH2O的组成,进行如下实验(假设每步反应、吸收均完全):

【查阅资料】aZnCO3•bZn(OH)2•cH2O受热分解生成ZnO、H2O、CO2三种产物.
(6)写出装置B中发生反应的化学方程式aZnCO3•bZn(OH)2•cH2O$\frac{\underline{\;\;△\;\;}}{\;}$(a+b)ZnO+aCO2↑+(b+c)H2O .
现称取35.9g aZnCO3•bZn(OH)2•cH2O在B装置中进行完全煅烧,测得装置C和D的质量分别增重7.2g和4.4g.
【实验分析及数据处理】
(7)装置A的作用是除去空气中二氧化碳和水.
(8)根据上述数据,则生成ZnO的质量为24.3 g;a:b:c=1:2:2.
(9)若没有E装置,则测得的a值偏大(填“偏大”、“偏小”或“不变”).
 铁、铜、银、锌是生活中常见的金属,请根据所学知识回答下列问题.
铁、铜、银、锌是生活中常见的金属,请根据所学知识回答下列问题. 老师在第十单元课题2“酸和碱的中和反应”课堂演示了酸碱中和滴定实验,但对实验进行了改进,并对两个问题进行了讨论.
老师在第十单元课题2“酸和碱的中和反应”课堂演示了酸碱中和滴定实验,但对实验进行了改进,并对两个问题进行了讨论.
 ,则x=38,锶元素的氯化物的化学式为SrCl2.
,则x=38,锶元素的氯化物的化学式为SrCl2.