题目内容
若用20g表面部分已氧化的镁带,跟足量稀硫酸反应,生成氢气0.4g,则该镁带中单质镁的质量分数是多少?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据氢气的质量可以计算单质镁的质量,从而可以计算出镁带中单质镁的质量分数.
解答:解:设镁的质量为x
Mg+H2SO4=MgSO4+H2↑
24 2
x 0.4g
=
x=4.8g
该镁带中单质镁的质量分数是
×100%=24%
答案:该镁带中单质镁的质量分数是24%
Mg+H2SO4=MgSO4+H2↑
24 2
x 0.4g
| 24 |
| 2 |
| x |
| 0.4g |
x=4.8g
该镁带中单质镁的质量分数是
| 4.8g |
| 20g |
答案:该镁带中单质镁的质量分数是24%
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
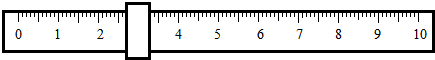
托盘天平调零后,在右盘衬纸上置氧化铜粉末,左盘衬纸上置1个5g砝码,游码标尺示数如图,此时天平平衡.则被称量的氧化铜实际质量为( )

| A、2.3g | B、2.7g |
| C、7.7g | D、8.2g |
下列氧气的用途①气焊 ②动植物呼吸 ③医疗 ④潜水 ⑤宇航,其中是利用氧气可以支持燃烧并放出热量的性质的是( )
| A、①②③ | B、①⑤ |
| C、①③④⑤ | D、①②③④⑤ |