题目内容
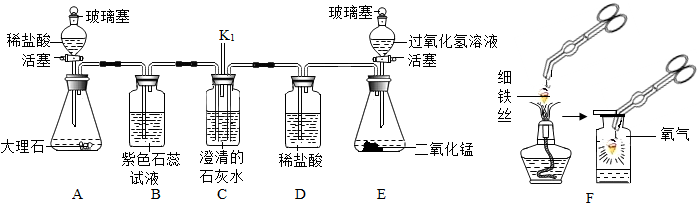
7.根据图回答问题.
(1)图中a的试管,b的仪器名称水槽.
(2)用高锰酸钾制取氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;收集氧气所选用的装置是C或E(填字母,下同),制取氧气所选用的装置是A(填字母,下同);
(3)用大理石和稀盐酸制取二氧化碳时,所选用的发生装置是B,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,实验室不用大理石和稀硫酸制取二氧化碳的原因是生成的硫酸钙微溶于水,阻碍反应的进行.
(4)图2所示装置有多种用途,下列说法正确的是ACD.
A.除去氧气中的水蒸气--瓶内盛放浓硫酸
B.检验二氧化碳气体--瓶内盛放氢氧化钠溶液
C.用排空气法收集氢气--气体从装置的b端通入
D.用排水法收集氧气--瓶内先装满水,气体从b端通入.
分析 试管是常用的反应容器,水槽是盛水的仪器;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;实验室不用大理石和稀硫酸制取二氧化碳的原因是:生成的硫酸钙微溶于水,阻碍反应的进行;图2所示装置有多种用途,下列说法正确的是:除去氧气中的水蒸气--瓶内盛放浓硫酸;用排空气法收集氢气--气体从装置的b端通入;用排水法收集氧气--瓶内先装满水,气体从b端通入;检验二氧化碳气体--瓶内盛放氢氧化钠溶液是错误的,因为二氧化碳是用澄清石灰水检验的.
解答 解:(1)试管是常用的反应容器,水槽是盛水的仪器,故答案为:试管;水槽;
(2)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;故答案为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;C或E;A;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;实验室不用大理石和稀硫酸制取二氧化碳的原因是:生成的硫酸钙微溶于水,阻碍反应的进行;故答案为:B;CaCO3+2HCl=CaCl2+H2O+CO2↑;生成的硫酸钙微溶于水,阻碍反应的进行;
(4)图2所示装置有多种用途,下列说法正确的是:除去氧气中的水蒸气--瓶内盛放浓硫酸;用排空气法收集氢气--气体从装置的b端通入;用排水法收集氧气--瓶内先装满水,气体从b端通入;检验二氧化碳气体--瓶内盛放氢氧化钠溶液是错误的,因为二氧化碳是用澄清石灰水检验的;故答案为:ACD;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| A. | 溶液具有均一、稳定的特征,所以均一、稳定的物质一定是溶液 | |
| B. | 单质是由同种元素组成的,但同种元素组成的物质不一定是单质 | |
| C. | 向某溶液中滴加氯化钡溶液,产生不溶于稀硝酸的白色沉淀,说明该溶液中可能存在SO${\;}_{4}^{2-}$ | |
| D. | 溶液中有晶体析出,其溶质质量减小,所以溶质的质量分数一定减小 |
| A. | 可用氮气或二氧化碳作为食品保护气以防腐 | |
| B. | 利用洗洁精的乳化原理清洗油污 | |
| C. | 可用灼烧闻气味的方法鉴别丝织品还是棉织品 | |
| D. | 镉大米(含重金属镉)可放心食用 |
| A. | 用稀盐酸除铁锈 | B. | 用钨做白炽灯泡的灯丝 | ||
| C. | 用熟石灰改良酸性土壤 | D. | 用纯碱发面蒸馒头 |
| A. |  读出液体体积 | B. |  铁丝在氧气中燃烧 | ||
| C. |  除去CO中的CO2 | D. |  滴管的使用 |