题目内容
20.①将燃着的镁条伸入装有二氧化碳气体的烧杯中,镁条继续燃烧,说明二氧化碳还具有的性质是助燃性.②镁在二氧化碳中燃烧的化学方程式为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
计算:2.4g镁在二氧化碳气体中完全燃烧,有多少碳生成?
分析 ①根据燃着的镁条伸入装有二氧化碳气体的烧杯,镁条继续燃烧进行解答即可;
②根据化学方程式和题中金属镁的质量进行计算.
解答 解:①燃着的镁条伸入装有二氧化碳气体的烧杯,镁条继续燃烧,说明二氧化碳还具有的性质是助燃性;
②设生成碳的质量为x
2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C
48 12
2.4g x
$\frac{48}{2.4g}$=$\frac{12}{x}$
x=0.6g
故答案为:①助燃性;
②生成碳的质量为0.6g.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的关系和准确性.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.下列符号中,表示两个氢原子的是( )
| A. | H2 | B. | 2H2 | C. | 2H+ | D. | 2H |
5.七氧化二氯(Cl2O7)和二氧化碳、二氧化硫一样均可以跟碱反应生成相应的盐和水,当七氧化二氯与氢氧化钠溶液恰好完全反应后,所得溶液中存在的阴离子是( )
| A. | ClO4- | B. | ClO3- | C. | ClO2- | D. | ClO- |
9.将5.6g铁粉加入到100g硫酸铜溶液中,恰好完全反应,则反应后所得溶液中溶质的质量分数为( )
| A. | 15.3% | B. | 32.4% | C. | 49.3% | D. | 52.6% |
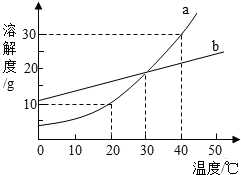 如图是a、b两种固体物质的溶解度曲线.
如图是a、b两种固体物质的溶解度曲线.

 A~F是初中化学常见的物质,它们存在如图所示的关系(“一”表示两物质间能反应,“→”表示一种物质转化成另一种物质.部分生成物和反应条件已略去).A、B、C三种物质中都含有碳元素,A为黑色固体;D、E、F三种物质中都含有钙元素,F可作干燥剂.请回答下列问题:
A~F是初中化学常见的物质,它们存在如图所示的关系(“一”表示两物质间能反应,“→”表示一种物质转化成另一种物质.部分生成物和反应条件已略去).A、B、C三种物质中都含有碳元素,A为黑色固体;D、E、F三种物质中都含有钙元素,F可作干燥剂.请回答下列问题: