题目内容
11.如图A、B、C、D是四种粒子的结构示意图,E是元素周期表中的一格.请回答下列问题:
(1)在A、B、C、D四种粒子中,属于同种元素的是A、B(填序号,下同),属于离子的是B;X值等于8;
(2)A粒子的化学性质与BCD中哪一种粒子的化学性质相似C(填序号),D元素位于周期表中第3周期;
(3)钙的相对原子质量是40.08.
分析 (1)根据元素的定义、核内质子数与核外电子数的关系分析;
(2)根据元素的性质与原子最外层电子数的关系、原子的电子层数等于元素的周期数分析回答;
(3)根据元素周期表中一个格所表示的含义分析回答.
解答 解:(1)在A、B、C、D四种粒子中,A、B的质子数相同,属于同种元素;在B中,质子数=8<电子数=10,属于离子;在原子中,质子数等于核外电子数,所以X值等于18-2-8=8.
(2)A粒子与粒子的最外层电子数相同,化学性质相似;D元素的原子的核外有3个电子层,位于周期表中第3周期;.
(3)由元素周期表一个格的含义可知,钙的相对原子质量是40.08.
故答为:(1)A、B;B;8. (2)C;3.(3)40.08.
点评 本题考查了结构示意图的意义、元素周期表的应用,较为简单.完成此题,可以依据已有的知识即可进行解答.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
2.下列归纳总结完全正确的一组是( )
| A.物质用途 ①黄金--装饰品 ②熟石灰--改良酸性土壤 ③氯化钠--调味品 | B.安全知识 ①点燃可燃性气体前一定要验纯 ②鉴别化学药品时可以品尝 ③居室装修时应常开窗通风,防止甲醛中毒 |
| C.合理利用资源 ①随意大量使用塑料袋 ②过量使用农药、化肥提高农业产量 ③钢铁表面刷上油漆,防止钢铁生锈 | D.物质分类 ①纯碱属于碱类 ②塑料属于合成材料 ③生铁属于合金 |
| A. | A | B. | B | C. | C | D. | D |
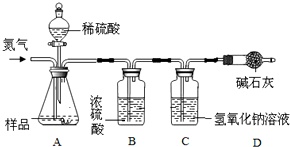
19.氢氧化钠固体及溶液在空气中很容易发生变质生成碳酸钠.
(1)甲同学在实验室里发现一瓶敞口放置的氢氧化钠溶液,对其变质情况进行了如下探究.
【猜想与假设】该氢氧化钠溶液已部分变质.
【实验与结论】
【拓展探究】甲同学又尝试通过实验除去该氢氧化钠溶液中含有的碳酸钠,方案如下:
向该溶液中加入适量氢氧化钙,反应后,经过滤操作,即可除去该氢氧化钠溶液中含有的杂质.
(2)乙同学在实验室里发现少量部分变质的氢氧化钠固体,尝试通过实验测定其中碳酸钠的质量分数.
【设计和进行实验】乙同学设计了如图所示的实验装置(铁架台、铁夹等固定用装置已略去,碱石灰是固体氢氧化钠和生石灰的混合物),取10.0g待测样品,进行实验.
实验步骤如图:
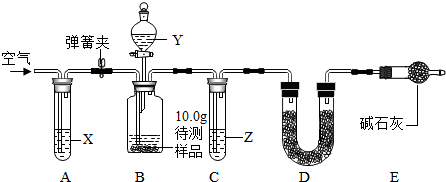
a.连接好装置,并检查气密性;
b.打开弹簧夹,缓缓通入一段时间空气;
c.称量装置D的质量为83.4g;
d.关闭弹簧夹,慢慢滴加Y溶液,至不再产生气泡为止;
e.打开弹簧夹,再次缓缓通入一段时间空气;
f.再次称量装置D的质量为84.5g.
【交流讨论】
①试剂X、Y、Z依次最适宜选用C(选填字母).
A.氢氧化钠溶液 浓盐酸 浓硫酸 B.澄清石灰水 稀盐酸 稀硫酸
C.氢氧化钠溶液 稀硫酸 浓硫酸 D.浓硫酸 稀硫酸 氢氧化钠溶液
②步骤e中通入空气的作用是将B中产生的二氧化碳全部赶到D装置中.
③若没有装置C或E,则会导致测定结果偏大(选填“偏大”、“偏小”或“无影响”)
【数据处理】根据实验中测得的有关数据,计算部分变质的氢氧化钠固体中碳酸钠的质量分数是26.5%.
(1)甲同学在实验室里发现一瓶敞口放置的氢氧化钠溶液,对其变质情况进行了如下探究.
【猜想与假设】该氢氧化钠溶液已部分变质.
【实验与结论】
| 实验步骤 | 实验现象 | 实验结论 |
| a.取少量该溶液于一支试管中,加入足量氯化钙溶液 | 有白色沉淀生成 | 该氢氧化钠溶液已变质 |
| b.将步骤a所得的液体过滤,取滤液于另一支试管中,滴加无色酚酞试液 | 酚酞试液变红 | 该氢氧化钠溶液已部分变质 |
向该溶液中加入适量氢氧化钙,反应后,经过滤操作,即可除去该氢氧化钠溶液中含有的杂质.
(2)乙同学在实验室里发现少量部分变质的氢氧化钠固体,尝试通过实验测定其中碳酸钠的质量分数.
【设计和进行实验】乙同学设计了如图所示的实验装置(铁架台、铁夹等固定用装置已略去,碱石灰是固体氢氧化钠和生石灰的混合物),取10.0g待测样品,进行实验.
实验步骤如图:

a.连接好装置,并检查气密性;
b.打开弹簧夹,缓缓通入一段时间空气;
c.称量装置D的质量为83.4g;
d.关闭弹簧夹,慢慢滴加Y溶液,至不再产生气泡为止;
e.打开弹簧夹,再次缓缓通入一段时间空气;
f.再次称量装置D的质量为84.5g.
【交流讨论】
①试剂X、Y、Z依次最适宜选用C(选填字母).
A.氢氧化钠溶液 浓盐酸 浓硫酸 B.澄清石灰水 稀盐酸 稀硫酸
C.氢氧化钠溶液 稀硫酸 浓硫酸 D.浓硫酸 稀硫酸 氢氧化钠溶液
②步骤e中通入空气的作用是将B中产生的二氧化碳全部赶到D装置中.
③若没有装置C或E,则会导致测定结果偏大(选填“偏大”、“偏小”或“无影响”)
【数据处理】根据实验中测得的有关数据,计算部分变质的氢氧化钠固体中碳酸钠的质量分数是26.5%.
16.为测定某AgNO3溶液的溶质质量分数,某兴趣小组的同学分五次进行了实验,每次向100g AgNO3溶液加入一定量的铜粉,充分反应后过滤、洗涤、干燥.测得相关数据如下:
(1)上表中数据a的值为0.8;
(2)上述实验中第四(填序号)次实验铜粉与AgNO3溶液恰好完全反应;
(3)计算该AgNO3溶液的溶质质量分数;
(4)第五次实验所得滤液的质量为96.2g.
| 实验序号 | 一 | 二 | 三 | 四 | 五 |
| 加入铜粉质量/g | 0.4 | a | 1.2 | 1.6 | 2 |
| 所得滤渣质量/g | 1.35 | 2.7 | 4.05 | 5.4 | 5.8 |
(2)上述实验中第四(填序号)次实验铜粉与AgNO3溶液恰好完全反应;
(3)计算该AgNO3溶液的溶质质量分数;
(4)第五次实验所得滤液的质量为96.2g.
3.X是合成维生素A的重要原料.工业上用物质甲和乙在一定条件下反应生成物质丙和X,甲、乙和丙的微观示意图见下表.
该反应中甲、乙、丙的质量比为23:17:1.下列判断不正确的是( )
| 物质 | 甲 | 乙 | 丙 | X | |
| 微观 示意图 |  |  |  | ? |  |
| A. | X属于化合物 | |
| B. | 该反应方程式中乙与丙的化学计量数之比为2:3 | |
| C. | 物质X中含三种元素 | |
| D. | 该反应为置换反应 |
20.保护环境,节约资源,从我做起.下列做法不符合这一理念的是( )
| A. | 使用降解塑料 | B. | 推广乙醇汽油 | ||
| C. | 减少燃煤使用 | D. | 废旧电池掩埋在土壤中 |
1. 2016第七届井冈山杜鹃花节吸引了很多游客,走在杜鹃山的路上,阵阵花香,沁人心脾.花香四溢的现象说明( )
2016第七届井冈山杜鹃花节吸引了很多游客,走在杜鹃山的路上,阵阵花香,沁人心脾.花香四溢的现象说明( )
 2016第七届井冈山杜鹃花节吸引了很多游客,走在杜鹃山的路上,阵阵花香,沁人心脾.花香四溢的现象说明( )
2016第七届井冈山杜鹃花节吸引了很多游客,走在杜鹃山的路上,阵阵花香,沁人心脾.花香四溢的现象说明( )| A. | 分子是不断运动的 | B. | 分子是由原子构成的 | ||
| C. | 分子具有一定的质量 | D. | 分子之间有一定的间隔 |