题目内容
19.某密闭容器内有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量如表.下列说法正确的是( )| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(克) | 4 | 1 | 10 | 2 |
| 反应后质量(克) | m | 5 | 4 | 8 |
| A. | m为1克 | |
| B. | 该反应为化合反应 | |
| C. | 甲与乙的相对分子质量比一定是1:1 | |
| D. | 参加反应的甲与丙的质量比为2:3 |
分析 根据质量守恒定律和图表中的数据先求出“待测”处的质量,然后对选项逐一进行分析,即可正确选择.
解答 解:A、根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.故反应后m的质量为:(4+1+10+2)-(5+4+8)=0.故A说法不正确;
B、由图示数值可知,反应后甲、丙质量减少,所以甲、丙为反应物,比较乙、丁的质量在反应前后的变化情况可以知道乙、丁的质量均增加,所以可以判断乙、丁均为生成物.故该反应不可能是化合反应.故B说法不正确;
C、根据题意,甲与乙的反应质量之比为(4g-0g):(5g-1g)=1:1,但因为反应式中甲与乙的系数之比未知,故无法判断其相对分子质量比,故C说法不正确;
D、参加反应的甲与丙的质量比是:(4g-0):(10g-4g)=4g:6g=2:3.故D说法正确.
故选D.
点评 本题主要考查学生运用质量守恒定律解答问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10.规范的实验操作是实验成功的关键.下列实验操作正确的是( )
| A. | 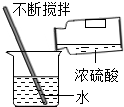 | B. | 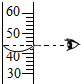 | C. | 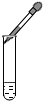 | D. | 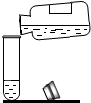 |
14.下列各组微粒中,属于同一种元素的是( )
| A. | H2O和H2O2 | B. | Co和CO | C. | H和He | D. | Na和Na+ |
4. 某科学兴趣小组的同学按照课本上的实验装置做“测定空气中氧气的体积分数”实验(如图1所示),但测出的氧气的体积分数明显小于$\frac{1}{5}$.请你参与探究:
某科学兴趣小组的同学按照课本上的实验装置做“测定空气中氧气的体积分数”实验(如图1所示),但测出的氧气的体积分数明显小于$\frac{1}{5}$.请你参与探究:
【提出问题】造成误差的原因是什么?如何改进课本上的实验装置?
【查阅资料】红磷、白磷的一些性质如表:
【猜想与假设】
甲同学:可能是导管内原含有空气,后来留有吸入的水,影响实验的准确性.
乙同学:可能是瓶内残留气体中还有氧气.
你还能作出的猜想是集气瓶未冷却至室温就打开了弹簧夹(或装置气密性不好).
【交流与讨论】
(1)丙同学认为用木炭代替红磷,就可以消除误差,你认为他的猜想不合理,(填“合理”或“不合理”)理由是木炭可以和氧气反应生成二氧化碳气体,不能产生压强差.
(2)他们利用金属的导热性,对课本上的实验装置进行了图2所示的改进(其他仪器忽略).
①甲同学提出应把红磷换为白磷,理由是磷的着火点低,可以较容易的发生燃烧.
②与课本上的实验装置相比较,该装置的一个优点是实验误差小,不会污染空气.
【探究与反思】
(1)为了验证乙同学的猜想,将铜粉放在残余气体中加热,观察到铜粉变黑色,证明乙同学的猜想合理(填“合理”或“不合理”)
(2)大家用改进的实验装置(如图2所示)进行实验,待玻璃管冷却、管内白色的烟幕消失时,左玻璃管内的液面上升了1格,得到了较准确的结果.左玻璃管上端的白色固体的主要成分可能是五氧化二磷.
 某科学兴趣小组的同学按照课本上的实验装置做“测定空气中氧气的体积分数”实验(如图1所示),但测出的氧气的体积分数明显小于$\frac{1}{5}$.请你参与探究:
某科学兴趣小组的同学按照课本上的实验装置做“测定空气中氧气的体积分数”实验(如图1所示),但测出的氧气的体积分数明显小于$\frac{1}{5}$.请你参与探究:【提出问题】造成误差的原因是什么?如何改进课本上的实验装置?
【查阅资料】红磷、白磷的一些性质如表:
| 颜色、状态 | 熔点/℃ | 着火点/℃ | 密度/ (g/cm3) | |
| 红磷 | 暗红色固体 | 590 | 240 | 2.34 |
| 白磷 | 白色或黄色固体 | 44.1 | 40 | 1.82 |
甲同学:可能是导管内原含有空气,后来留有吸入的水,影响实验的准确性.
乙同学:可能是瓶内残留气体中还有氧气.
你还能作出的猜想是集气瓶未冷却至室温就打开了弹簧夹(或装置气密性不好).
【交流与讨论】
(1)丙同学认为用木炭代替红磷,就可以消除误差,你认为他的猜想不合理,(填“合理”或“不合理”)理由是木炭可以和氧气反应生成二氧化碳气体,不能产生压强差.
(2)他们利用金属的导热性,对课本上的实验装置进行了图2所示的改进(其他仪器忽略).
①甲同学提出应把红磷换为白磷,理由是磷的着火点低,可以较容易的发生燃烧.
②与课本上的实验装置相比较,该装置的一个优点是实验误差小,不会污染空气.
【探究与反思】
(1)为了验证乙同学的猜想,将铜粉放在残余气体中加热,观察到铜粉变黑色,证明乙同学的猜想合理(填“合理”或“不合理”)
(2)大家用改进的实验装置(如图2所示)进行实验,待玻璃管冷却、管内白色的烟幕消失时,左玻璃管内的液面上升了1格,得到了较准确的结果.左玻璃管上端的白色固体的主要成分可能是五氧化二磷.
11. 用如图装置电解水,一段时间后的现象如图所示.对该实验的描述错误的是( )
用如图装置电解水,一段时间后的现象如图所示.对该实验的描述错误的是( )
 用如图装置电解水,一段时间后的现象如图所示.对该实验的描述错误的是( )
用如图装置电解水,一段时间后的现象如图所示.对该实验的描述错误的是( )| A. | 甲试管中收集到的是一种可燃性气体 | |
| B. | 该实验能证明水是由氢元素和氧元素组成的 | |
| C. | 乙试管中收集到的气体能使带火星的木条复燃 | |
| D. | 甲、乙两试管内收集到的气体的体积比约为1:2 |
8.进行化学实验时必须要有安全意识,下列做法错误的是( )
| A. | 被玻璃割伤手后,先取出伤口里的玻璃片,再用稀过氧化氢溶液擦洗,然后敷药包扎 | |
| B. | 制取蒸馏水时,为了防止瓶内产生暴沸现象,应向烧瓶内加入几片碎瓷片 | |
| C. | 温度计摔坏导致水银散落到地面上,应立即用水冲洗水银 | |
| D. | 滴瓶中的滴管用后不用清洗,直接放到原滴瓶中 |
9.下列事实解释错误的是( )
| 选项 | 事实 | 解释 |
| A | 酒精灯不用时,需用灯帽盖好 | 酒精分子在不断地运动到空气中 |
| B | 水结成冰时体积变大 | 水分子之间的间隔变大 |
| C | 白磷的着火点比红磷的着火点低 | 磷原子的内部结构不同 |
| D | 给装水的纸杯加热,纸杯开始时完好无损 | 温度没有达到纸的着火点 |
| A. | A | B. | B | C. | C | D. | D |