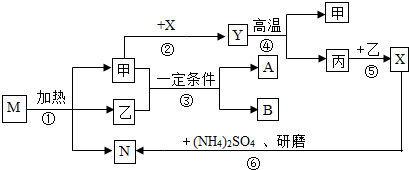
题目内容
6.溶液甲中的溶质为Fe2(SO4)3、CuSO4及H2SO4,利用以下实验可制取碳酸亚铁并回收铜.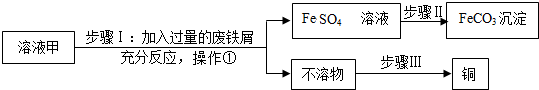
(1)操作1中,所用玻璃仪器有漏斗、玻璃棒、烧杯.
(2)步骤Ⅱ中加入一种试剂可实现其转化,该试剂可以是Na2CO3(填化学式).
(3)步骤Ⅲ回收铜的实验操作包括:①过滤 ②洗涤 ③加足量稀硫酸 ④干燥,正确的操作排序是③①②④(填序号).
(4)若废铁屑含有少量铁锈,对实验结果无(填“有”或“无”)影响.
分析 根据实验操作确定所有的仪器;根据铁的金属活动性排在氢、铜的前面,能发生置换反应;根据硫酸钠可溶,碳酸亚铁不可溶解答;根据回收铜的步骤解答;根据铁锈与硫酸反应生成硫酸铁,硫酸铁和铁会生成硫酸亚铁分析.
解答 解:(1)操作①是过滤,所用的玻璃仪器有烧杯、漏斗和玻璃棒,故填:漏斗;
(2)步骤Ⅱ中加入一种试剂可实现其转化,该试剂可以是Na2CO3,碳酸钠与硫酸亚铁反应生成碳酸亚铁沉淀;故填:Na2CO3;
(3)步骤Ⅲ回收铜的实验操作因不溶物中含有铜和铁,先加足量稀硫酸,与铁反应,然后过滤则不容的部分为铜,再经过洗涤、干燥得到铜;故填:③①②④;
(4)溶液中含有硫酸铜,硫酸铜和加入的铁屑反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=Cu+FeSO4;步骤Ⅰ中,废铁屑含有少量铁锈,对产物的成分没有影响,原因是铁锈与硫酸反应生成硫酸铁,硫酸铁和铁会生成硫酸亚铁;故填:无.
点评 本题是一道常规的资源回收题,解题的方法是对设计方案所涉及的化学反应要能明确,并进而对反应物生成物作出判断,此题属基础性回收实验题.

练习册系列答案
相关题目
16.对下列事实的微观解释正确的是( )
| 选项 | 事实 | 解释 |
| A | CO有毒,而CO2无毒 | 两物质的组成元素不同,分子构成不同 |
| B | KNO3溶液能导电 | 溶液中存在自由移动的粒子 |
| C | KCl溶液和KMnO4溶液颜色不同 | 溶液中阴离子不同 |
| D | 稀硫酸和稀盐酸具有相似的化学性质 | 因为它们都含氢元素 |
| A. | A | B. | B | C. | C | D. | D |
17.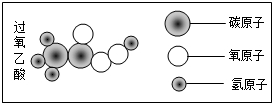 日本大地震后,我国救援人员出发时携带了大量过氧乙酸进行消毒.过氧乙酸分子模型如图,下列说法正确的是( )
日本大地震后,我国救援人员出发时携带了大量过氧乙酸进行消毒.过氧乙酸分子模型如图,下列说法正确的是( )
 日本大地震后,我国救援人员出发时携带了大量过氧乙酸进行消毒.过氧乙酸分子模型如图,下列说法正确的是( )
日本大地震后,我国救援人员出发时携带了大量过氧乙酸进行消毒.过氧乙酸分子模型如图,下列说法正确的是( )| A. | 过氧乙酸是由三种原子构成的 | |
| B. | 一个过氧乙酸分子中的质子数是60 | |
| C. | 过氧乙酸中碳元素与氧元素的质量之比为1:2 | |
| D. | 过氧乙酸的化学式为CH3COOH |
14.“二氧化碳的制取、收集和验满”.如图是他的主要实验步骤,其中操作有误的是( )
| A. | 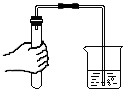 检查气密性 检查气密性 | B. | 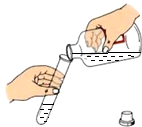 加入稀盐酸 | C. | 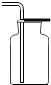 收集二氧化碳 | D. | 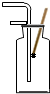 二氧化碳验满 |
1.下列说法正确的是( )
| A. | 焦炭在炼铁中的作用只是提供高温 | |
| B. | 20℃的氢氧化钙的溶解度小于60℃氢氧化钙的溶解度 | |
| C. | 钢铁在海水中比在河水中更易腐蚀,主要原因是海水含盐量高于河水 | |
| D. | 将质量分数为98%的硫酸加入等体积的水中,所得硫酸的质量分数等于49% |
1.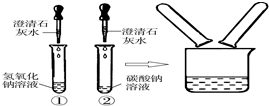 在化学实验技能考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小红等几位同学进行了如图所示的实验.
在化学实验技能考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小红等几位同学进行了如图所示的实验.
(1)写出试管②中碳酸钠与氢氧化钙反应的化学方程式:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(2)实验结束后,小红同学将①、②两支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行了过滤,小红等几位同学对滤液的成分又进行了探究.
【提出问题】滤液中除水外还含有哪些物质?
【猜想】小红认为:只含氢氧化钠;
小明认为:可能含有氢氧化钠、碳酸钠和氢氧化钙;
小亮认为:可能含有氢氧化钠和碳酸钠;
你认为还可能是氢氧化钠和氢氧化钙(写一种猜想).
【讨论】你认为小红、小明、小亮三位同学中谁的猜想不合理,请说明理由.小明猜想不合理,因为Na2CO3和Ca(OH)2能发生反应,不能共存.
【实验设计】设计一个简单的实验证明你的猜想正确.
【实验分析】小亮同学针对自己的猜想进行了如下实验:
你认为小亮同学对实验结果判断是否正确?请说明理由.不正确,因有氢氧化钠存在,滴入几滴稀盐酸量太少,不会立即出现气泡,但Na2CO3有可能存在.
【反思拓展】
①在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑所加的反应物是否过量;
②通过以上探究,你认为应怎样处理上述实验后的废液才能倒入下水道?在废液中加酸至溶液的pH=7.
 在化学实验技能考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小红等几位同学进行了如图所示的实验.
在化学实验技能考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小红等几位同学进行了如图所示的实验.(1)写出试管②中碳酸钠与氢氧化钙反应的化学方程式:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(2)实验结束后,小红同学将①、②两支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行了过滤,小红等几位同学对滤液的成分又进行了探究.
【提出问题】滤液中除水外还含有哪些物质?
【猜想】小红认为:只含氢氧化钠;
小明认为:可能含有氢氧化钠、碳酸钠和氢氧化钙;
小亮认为:可能含有氢氧化钠和碳酸钠;
你认为还可能是氢氧化钠和氢氧化钙(写一种猜想).
【讨论】你认为小红、小明、小亮三位同学中谁的猜想不合理,请说明理由.小明猜想不合理,因为Na2CO3和Ca(OH)2能发生反应,不能共存.
【实验设计】设计一个简单的实验证明你的猜想正确.
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入碳酸钠溶液 | 试管中出现白色浑浊 | 你的猜想正确 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入几滴稀盐酸 | 没有气泡产生 | 自己的猜想不成立 |
【反思拓展】
①在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑所加的反应物是否过量;
②通过以上探究,你认为应怎样处理上述实验后的废液才能倒入下水道?在废液中加酸至溶液的pH=7.
18.钠盐种类较多.在实验室里,钠盐通常都摆放在同一药品柜中.化学兴趣小组在整理药品柜时,发现某试剂瓶外壁两边贴上了新旧两个标签,分别是“Na2SO4溶液”、“Na2CO3溶液”,小组同学认为可能存在没看清试剂标签的情况下,将两瓶试剂混合清理,立即对溶液的成分进行了探究.请你完成以下探究过程,并将①~⑤处的答
案填入答题卡相应位置.
【提出问题】该试剂瓶内溶质的化学成分是什么?
【提出猜想】猜想I:溶质仅为Na2SO4;
猜想II:溶质仅为Na2CO3;
猜想III:溶质为Na2SO4和Na2CO3;.
【实验探究】
【问题讨论】试写出加入过量的BaCl2溶液后,生成不溶于硝酸的白色沉淀的化学方程式BaCl2+Na2SO4═BaSO4↓+2NaCl.
案填入答题卡相应位置.
【提出问题】该试剂瓶内溶质的化学成分是什么?
【提出猜想】猜想I:溶质仅为Na2SO4;
猜想II:溶质仅为Na2CO3;
猜想III:溶质为Na2SO4和Na2CO3;.
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| 1、取少量样品于一支洁净试管中,加入足量稀硫酸. | 有气泡产生 | 猜想I不成立. |
| 2、取少量样品于另一只洁净试管中,向其中加入过量的BaCl2溶液,过滤,向所得沉淀中加入足量稀硝酸. | 先产生白色沉淀;加入稀硝酸后,有气泡产生,白色沉淀部分溶解. | 猜想Ⅲ成立. |
19.某密闭容器内有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量如表.下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(克) | 4 | 1 | 10 | 2 |
| 反应后质量(克) | m | 5 | 4 | 8 |
| A. | m为1克 | |
| B. | 该反应为化合反应 | |
| C. | 甲与乙的相对分子质量比一定是1:1 | |
| D. | 参加反应的甲与丙的质量比为2:3 |