题目内容
12.图象分别与选项中的操作相对应,合理的是( )| A. | 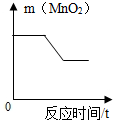 向一定质量的MnO2固体中加入一定量的过氧化氢溶液 | |
| B. | 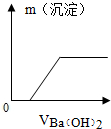 向一定量的HCl与Na2SO4混合溶液中不断加入Ba(OH)2溶液 | |
| C. | 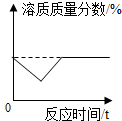 室温下,向一定质量的饱和石灰水中加入一定量的氧化钙 | |
| D. | 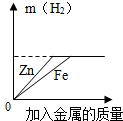 向两份完成相同的稀硫酸中,不断加入铁和锌 |
分析 A、根据二氧化锰是该反应的催化剂分析;
B、根据复分解反应发生的条件及Na2SO4与Ba(OH)2反应生成硫酸钡沉淀进行分析;
C、氧化钙和水反应放出大量的热,而氢氧化钙的溶解度随温度的升高而减小,所以开始反应时溶液中的溶质的质量会减小;
D、铁和锌都能与稀硫酸反应生成氢气,但相同质量的硫酸,所用锌应比铁多;
解答 解:A、在该反应中,二氧化锰是催化剂,反应的质量一直不变,故A错误;
B、向Na2SO4与盐酸的混合溶液中慢慢滴入Ba(OH)2溶液,由于Na2SO4不与HCl反应,Na2SO4与Ba(OH)2反应生成不溶于盐酸的硫酸钡沉淀,所以沉淀的生成应从零刻度开始.故B错误;
C、氧化钙和水反应放出大量的热,而氢氧化钙的溶解度随温度的升高而减小,所以开始反应时溶液中的溶质的质量分数会减小,但随着温度恢复,溶液中的质量分数会回到原来的水平,故正确;
D、铁和锌都能与稀硫酸反应生成氢气,但相同质量的硫酸完全反应,所用金属锌比铁多.故D错误;
故选C.
点评 解答此类问题时,一定要注意到纵横坐标轴的说明文字,这是对曲线所反应规律判断的依据,不可仅凭经验去解答.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
2.工业上用氨气(NH3)制取硝酸(HNO3),工业流程为:
①4NH3+5O2$\frac{\underline{\;\;△\;\;}}{\;}$4NO+6H2O
②2NO+O2═2NO2
③3NO2+H2O═2HNO3+NO,下列判断不正确的是( )
①4NH3+5O2$\frac{\underline{\;\;△\;\;}}{\;}$4NO+6H2O
②2NO+O2═2NO2
③3NO2+H2O═2HNO3+NO,下列判断不正确的是( )
| A. | ②为化合反应 | |
| B. | 一氧化氮(NO)的化学性质稳定 | |
| C. | 上述含氮物质中氮元素的化合价有-3,+2,+4,+5 | |
| D. | 制取硝酸过程中产生的NO可循环使用 |
20.属于氮肥的是( )
| A. | KCl | B. | CO(NH2)2 | C. | K2CO3 | D. | Ca(H2PO4)2 |
7.配制50g 10%的氯化钠溶液时,操作正确的是( )
| A. | 电子天平先调零,然后放烧杯称取氯化钠固体 | |
| B. | 用10mL量筒量取水 | |
| C. | 将配制好的溶液装入细口瓶中,塞好瓶塞 | |
| D. | 最后贴上标签,注上“50g 10%的氯化钠溶液” |
4.碳酸氢铵(NH4HCO3)是一种氮肥,受热易分解使肥效损失,因此应在避光阴凉处保存,碳酸氢铵分解的化学方程式是NH4HCO3$\stackrel{△}{→}$X↑+CO2+H2O,其中X的化学式是( )
| A. | NHO3 | B. | NO | C. | NH3 | D. | CO |
1.物质中含原子个数最多的是( )
| A. | 2克H2 | B. | 0.5mol O2 | ||
| C. | 1.5mol Fe | D. | 6.02×1023个CO2分子 |

 化学是以实验为主的学科,根据实验1、实验2回答问题:
化学是以实验为主的学科,根据实验1、实验2回答问题: