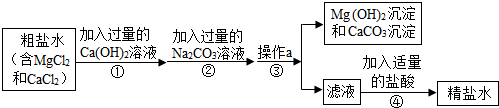
题目内容
(1)从微观角度看物质的变化是化学的思维方式之一.下面两幅示意图分别表示生成氯化钠的不同化学反应.请根据图示回答相关问题:

①图1是金属钠与氯气反应生成氯化钠的微观示意图.由图1可知,元素的化学性质与其微粒的 (填字母序号)有密切关系.
A.最外层电子数 B.内层电子数 C.电子层数 D.核电荷数
②图2描述了NaOH溶液与盐酸反应的微观实质是 .
(2)用质量分数为6%的氯化钠溶液(密度为1.04g/cm3),配制100g质量分数为3%的氯化钠溶液.配制过程为:
①计算(计算结果保留一位小数):需6%的氯化钠溶液 mL(计算的依据是 ),水 g.
②量取;③ ;④装瓶、贴标签.

①图1是金属钠与氯气反应生成氯化钠的微观示意图.由图1可知,元素的化学性质与其微粒的
A.最外层电子数 B.内层电子数 C.电子层数 D.核电荷数
②图2描述了NaOH溶液与盐酸反应的微观实质是
(2)用质量分数为6%的氯化钠溶液(密度为1.04g/cm3),配制100g质量分数为3%的氯化钠溶液.配制过程为:
①计算(计算结果保留一位小数):需6%的氯化钠溶液
②量取;③
考点:核外电子在化学反应中的作用,一定溶质质量分数的溶液的配制,中和反应及其应用
专题:物质的微观构成与物质的宏观组成,溶液、浊液与溶解度,常见的酸 酸的通性
分析:(1)①依据原子的最外层电子数与元素的性质的关系分析判断;②根据中和反应的实质对化学式或离子情况进行判断即可;
(2)根据溶液配制的步骤以及溶质质量分数公式进行解答.
(2)根据溶液配制的步骤以及溶质质量分数公式进行解答.
解答:解:(1)①依据金属钠与氯气反应生成氯化钠的微观示意图可知,该变化过程中两种原子的最外层电子数都发生了变化,所以可知元素的化学性质与原子的最外层电子数有密切关系;
②依据氢氧化钠能够电离出钠离子和氢氧根离子,盐酸能够电离出氢离子和氯离子,所以由图可知NaOH溶液与盐酸反应的微观实质是OH-与H+结合生成 H2O分子;
(2)用质量分数为6%的氯化钠溶液(密度为1.04g/cm3),配制100g质量分数为3%的氯化钠溶液.配制过程为:
①计算:设需6%的氯化钠溶液的体积为v,
利用溶液稀释前后溶质质量不变可知:
则v×1.04g/cm3×6%=100g×3%
v=48.1mL
水的质量=100g-48.1mL×1.04g/cm3=50.0g
②量取;③混匀;④装瓶、贴标签.
故答案为:
(1)①A;②OH-与H+结合生成 H2O分子;
(2)①48.1;稀释前后溶质质量不变;50.0;②混匀.
②依据氢氧化钠能够电离出钠离子和氢氧根离子,盐酸能够电离出氢离子和氯离子,所以由图可知NaOH溶液与盐酸反应的微观实质是OH-与H+结合生成 H2O分子;
(2)用质量分数为6%的氯化钠溶液(密度为1.04g/cm3),配制100g质量分数为3%的氯化钠溶液.配制过程为:
①计算:设需6%的氯化钠溶液的体积为v,
利用溶液稀释前后溶质质量不变可知:
则v×1.04g/cm3×6%=100g×3%
v=48.1mL
水的质量=100g-48.1mL×1.04g/cm3=50.0g
②量取;③混匀;④装瓶、贴标签.
故答案为:
(1)①A;②OH-与H+结合生成 H2O分子;
(2)①48.1;稀释前后溶质质量不变;50.0;②混匀.
点评:此题是对物质间反应的微观知识的考查,解题的关键是明确微观图示的有关含义掌握有关的分子结构情况.

练习册系列答案
相关题目
香蕉等水果具有芳香气味,是因为其中含有乙酸乙酯(C4H8O2)等物质.下列关于乙酸乙酯的说法不正确的是( )
| A、乙酸乙酯属于氧化物 |
| B、每个分子由4个碳原子、8个氢原子和2个氧原子构成 |
| C、乙酸乙酯中碳、氢、氧三种元素质量比为6:1:4 |
| D、乙酸乙酯的相对分子质量为88 |
下列有关燃烧实验现象的描述中错误的是( )
| A、加热铜丝表面变黑,生成氧化铜 |
| B、铁丝在氧气中燃烧火星四射 |
| C、聚氯乙烯在空气中灼烧有刺激性气味 |
| D、硫在氧气中燃烧产生黄色火焰 |

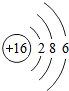 如图所表示的粒子符号为
如图所表示的粒子符号为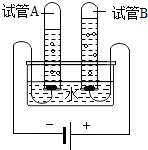 钓鱼岛是我国固有领土,钓鱼岛附近水域蕴藏着丰富的海底石油和天然气,并且是我国东海靖渔场,我国福建、浙江和台湾等地的渔民经常到这一带捕鱼.请回答:
钓鱼岛是我国固有领土,钓鱼岛附近水域蕴藏着丰富的海底石油和天然气,并且是我国东海靖渔场,我国福建、浙江和台湾等地的渔民经常到这一带捕鱼.请回答: