题目内容
4.(1)课堂上老师曾经给我们演示了如图1所示的实验,请回答下列问题:①对比分析铜片上白磷和水中白磷发生的现象,可以得出燃烧需要空气(氧气)的结论;
对比分析铜片上的红磷和白磷发生的现象,可以得出燃烧需要达到着火点的结论.
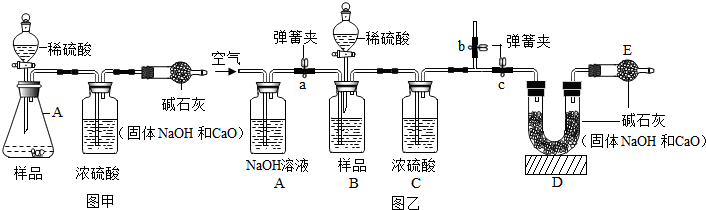
(2)金属资源属于不可再生资源.某同学用同规格且光亮洁净无锈的铁钉进行了如图2所示实验.

①一段时间后,铁钉表面生锈的是甲(填“甲”、“乙”或“丙”);由此可知,铁制品生锈的条件是铁与水和氧气共同作用.
②实验丙中为什么要用“刚煮沸并迅速冷却的蒸馏水”?除去水中溶解的氧气,使铁不能与氧气接触.
③铝的金属活动性比铁的活泼,但是铝的抗腐蚀性更强,原因是铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化.
分析 (1)了解物质燃烧的三个条件.即物质具有可燃性、与空气接触、达到着火点;并结合题意分析解答;
(2)①铁生锈的条件是:与氧气接触,有水参加;
②刚煮沸蒸馏水中没有氧气;
③根据铝的性质来分析.
解答 解:(1)铜片上的白磷能够燃烧是因为与氧气接触,并到达着火点;水中的白磷温度达到着火点,但没有与空气接触,不能燃烧.所以我们可以得出结论:燃烧需要空气(氧气).铜片上的白磷和红磷都与空气接触,但红磷的着火点是240℃,热水不能到这个温度,所以红磷不能燃烧.
故答案为:燃烧需要空气(氧气);燃烧需要达到着火点;
(2)①甲中铁钉与空气和水共同接触,乙中没有水,丙中没有氧气,故甲表面生锈,铁生锈的条件是:与氧气接触,有水参加,二者缺一不可,故答案为:甲;铁与水和氧气共同作用;
②实验丙中用“刚煮沸并迅速冷却的蒸馏水”是为了除去水中溶解的氧气,使铁不能与氧气接触,故答案为:除去水中溶解的氧气,使铁不能与氧气接触;
③通常情况下铝制品很耐腐蚀,这是因为铝在常温下与空气中的氧气发生化学反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化;故填:铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化.
点评 本题通过实验探究了物质燃烧的三个条件,考查了学生对知识的掌握以及应用分析解答问题的能力,要根据题意细心分析.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
1.下列变化中,后者一定包括前者的是( )
①化学变化、物理变化
②氧化反应、化合反应
③分解反应、化合反应
④状态变化、物理变化.
①化学变化、物理变化
②氧化反应、化合反应
③分解反应、化合反应
④状态变化、物理变化.
| A. | ①和② | B. | ③和④ | C. | 只有③ | D. | 只有④ |
18. 用“Y”形玻璃管(如图)做下列实验,在Ⅰ、Ⅱ支管中分别加入适量的物质及进行相应操作,不能达到实验目的是( )
用“Y”形玻璃管(如图)做下列实验,在Ⅰ、Ⅱ支管中分别加入适量的物质及进行相应操作,不能达到实验目的是( )
 用“Y”形玻璃管(如图)做下列实验,在Ⅰ、Ⅱ支管中分别加入适量的物质及进行相应操作,不能达到实验目的是( )
用“Y”形玻璃管(如图)做下列实验,在Ⅰ、Ⅱ支管中分别加入适量的物质及进行相应操作,不能达到实验目的是( )| A. | 白磷、红磷;放入60℃水中;验证不同的物质着火点不同 | |
| B. | 25℃的饱和硝酸钾溶液、饱和石灰水;放入5℃水中;验证不同的物质溶解度受温度影响不同 | |
| C. | 生石灰、熟石灰;分别加入适量的水并滴入无色酚酞;验证两种物质都是碱 | |
| D. | 湿润的蓝色石蕊试纸、干燥的蓝色石蕊试纸;分别同入二氧化碳;验证二氧化碳与水反应 |
14.下列有关环境污染的说法不正确的是( )
| A. | 二氧化碳是造成温室效应的主要气体 | |
| B. | “白色污染”是指一些白色垃圾造成的污染 | |
| C. | 二氧化硫是形成酸雨的气体 | |
| D. | 吸烟产生的一种有毒气体是一氧化碳 |

 利用如图所示的转化关系,请回答:
利用如图所示的转化关系,请回答: