题目内容
3.普通干电池在生活中的用途很广,其构造示意图如图1.回答下列问题:
(1)普通干电池用作照明时化学能转化为电能.
(2)电池中石墨表现出优良的导电性能;石墨与金刚石物理性质明显差异的原因是碳原子的排列方式不同.
(3)如图2是回收利用废旧普通干电池的一种工艺流程(不考虑废旧电池中实际存在的少量其他物质).
①分离回收铜帽,经净化处理后放入硝酸银溶液中,反应的化学方程式是Cu+2AgNO3=2Ag+Cu(NO3)2.
②滤液a中溶质的化学式是NH4Cl、ZnCl2.
③实验室中在加热和固体b存在的条件下制取氧气,反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
④氯化铵和尿素是重要的化学肥料,请简易鉴别氯化铵和尿素分别取少量化肥,在研钵里加少量熟石灰研磨,有刺激性氨味放出的为氯化铵,无氨味的是尿素.
分析 (1)根据能量的转化回答;
(2)石墨有优良的导电性、石墨与金刚石的碳原子的排列方式不同,据此分析回答;
(3)①根据铜与硝酸银的反应写出方程式;
②根据干电池的成分结合回收利用废旧普通干电池的工艺流程,分析滤液a中溶质;
③根据实验室制取氧气的反应原理分析回答;
④根据铵盐的鉴别方法分析回答.
解答 解:(1)普通干电池照明时化学能转化为电能.
(2)电池中石墨表现出优良的导电性能;石墨与金刚石物理性质明显差异的原因是:碳原子的排列方式不同.
(3)①分离回收铜帽,经净化处理后放入硝酸银溶液中,铜与硝酸银反应生成了硝酸铜和银,反应的化学方程式是:Cu+2AgNO3=2Ag+Cu(NO3)2.
②由干电池的成分可知,氯化铵、氯化锌是可溶性的,所以,滤液a中溶质的化学式是NH4Cl、ZnCl2.
③由回收利用废旧普通干电池的工艺流程可知,固体b是二氧化锰,实验室中在加热二氧化锰和存在的条件下制取氧气,应是加热氯化钾和二氧化锰的混合物制取氧气,反应的化学方程式是:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
④由于铵盐遇碱能放出氨气,所以,鉴别氯化铵和尿素的方法是:分别取少量化肥,在研钵里加少量熟石灰研磨,有刺激性氨味放出的为氯化铵,无氨味的是尿素.
故答为:(1)电能;(2)导电,碳原子的排列方式;(3)①Cu+2AgNO3=2Ag+Cu(NO3)2;②NH4Cl、ZnCl2;③2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;④分别取少量化肥,在研钵里加少量熟石灰研磨,有刺激性氨味放出的为氯化铵,无氨味的是尿素.
点评 本题通过回收利用废旧普通干电池的工艺流程考查了能量的转化、金属活动顺序、方程式的书写,铵盐的检验等知识,考查的知识点较多,难度不大.根据已有的知识即可解答.

| A. | Fe2O3→FeCl2 | B. | NaHCO3→CO2 | C. | CuCl2→Cu | D. | Na2CO3→NaOH |
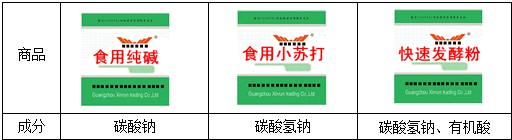
【提出问题】这种白色粉末是什么物质?
【查阅资料】通过对市场上相关产品进行调查,王霞发现了如图所示的三种商品.
【作出猜想】
猜想1:可能是食用纯碱;
猜想2:可能是食用小苏打;
猜想3:可能是快速发酵粉.
【设计实验】取少量白色粉末于试管中,加入适量蒸馏水,发现白色粉末溶解,无其他明显现象,实验结论是此粉未不是快速发酵粉,另取少量白色粉末于试管中,加入稀盐酸,有无色气体产生,王霞认为白色粉末是纯碱..
【实验反思】小明同学认为王霞同学根据上面的实验现象,不能得出白色粉末是纯碱,你若认为小明说法有道理,请用化学方程式解释不能得出结论的原因NaHCO3+HCl═NaCl+H2O+CO2↑;为了得到鉴别纯碱和小苏打的正确方法,王霞继续查找资料,发现它们有下列的性质.
| 性质 | 碳酸钠 | 碳酸氢钠 |
| 溶解性 | 20℃时溶解度21.6g,溶解时放热 | 20℃时溶解度9.8g,溶解时放热 |
| 加热 | 不分解 | 发生分解反应,分解产物为碳酸钠、二氧化碳和水. |
方案1:加入CaCl2溶液,碳酸钠与之反应生成沉淀,则有沉淀生成的为碳酸钠,反之为碳酸氢钠;
方案2:20℃时,在100克水中加入12克该白色粉末,充分溶解后,如果有白色固体剩余,则为碳酸钠,否则为碳酸氢钠.
在查找资料过程中,王霞同学还发现纯碱不是碱,是由于其水溶液显碱性而得名.现要验证纯碱溶液是否显碱性,请写出用pH试纸来测其pH值的操作过程把一小块试纸放在玻璃片上,用沾有待测溶液的玻璃棒点在试纸上,观察颜色,与比色卡对比,读数.
| A. | 干冰用于人工降雨 | |
| B. | 将燃着的木条伸入集气瓶,火焰立即熄灭,证明瓶内原有气体就是二氧化碳 | |
| C. | 二氧化碳气体通入紫色石蕊试液中,溶液变为蓝色 | |
| D. | 用块状石灰石和稀硫酸迅速制备大量二氧化碳 |
| 序号 | 物 质 | 选用试剂 | 操作 |
| A | CO2(CO) | O2 | 点燃 |
| B | NaOH溶液(Na2CO3) | 稀盐酸 | 加入试剂至不再产生气泡 |
| C | KNO3溶液(KOH) | H2SO4溶液 | 加入适量的试剂 |
| D | Cu(Fe) | 稀硫酸 | 加入适量的试剂,过滤 |
| A. | A | B. | B | C. | C | D. | D |
 过氧化钠(Na2O2)固体常温下与二氧化碳反应的化学方程式为2Na2O2+2CO2═2Na2CO3+O2.现将沾有Na2O2固体的棉花放入如图的烧杯中,先点燃蜡烛,再沿着烧杯壁缓慢倒入适量稀硫酸,使之与杯底的Na2CO3反应,发现蜡烛火焰熄灭,而沾有Na2O2固体的棉花一会儿后燃烧起来.下列从实验获得的信息中,你认为不正确的是( )
过氧化钠(Na2O2)固体常温下与二氧化碳反应的化学方程式为2Na2O2+2CO2═2Na2CO3+O2.现将沾有Na2O2固体的棉花放入如图的烧杯中,先点燃蜡烛,再沿着烧杯壁缓慢倒入适量稀硫酸,使之与杯底的Na2CO3反应,发现蜡烛火焰熄灭,而沾有Na2O2固体的棉花一会儿后燃烧起来.下列从实验获得的信息中,你认为不正确的是( )| A. | 蜡烛熄灭是因为杯底产生的CO2气体隔绝了氧气 | |
| B. | CO2不支持蜡烛燃烧,但能支持棉花燃烧 | |
| C. | Na2O2与CO2反应放热,使温度达到棉花的着火点 | |
| D. | 棉花燃烧证明“可燃物、氧气、温度达到着火点”是燃烧必须同时具备的条件 |
| 选项 | 实验目的 | 实验方案 |
| A | 分离Na2CO3和NaOH固体混合物 | 加入过量氢氧化钙溶液,过滤 |
| B | 除去NaCl固体中的少量Na2CO3 | 加入过量稀盐酸,充分反应后,蒸干 |
| C | 检验CO2气体中含有少量的CO | 将混合气体依次通过灼热的氧化铁和澄清石灰水,观察澄清石灰水的变化 |
| D | 鉴别蒸馏水、氯化钙溶液 | 用肥皂水检验,观察产生气泡的多少 |
| A. | A | B. | B | C. | C | D. | D |
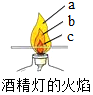 如图把一根火柴梗横放在酒精灯的火焰中,1-2秒后取出,观察到火柴梗在a处(填a、b、c)的部分最先碳化(变黑),说明外焰温度最高.
如图把一根火柴梗横放在酒精灯的火焰中,1-2秒后取出,观察到火柴梗在a处(填a、b、c)的部分最先碳化(变黑),说明外焰温度最高.