题目内容
5.现有一氧化碳和二氧化碳的混合气体20g,其中氧元素的质量分数为64%,先使该混合气体通过灼热的氧化铜再通过足量的澄清石灰水中,生成沉淀的质量为( )| A. | 60g | B. | 50g | C. | 40g | D. | 30g |
分析 先根据混合气体20g中氧元素的质量分数为60%,推算出含碳元素的质量分数,再根据碳元素都进入了碳酸钙中,根据碳元素的质量算出碳酸钙的质量.
解答 解:根据质量守恒定律,反应前后碳元素的质量不变,得
20g×(1-64%)=m(CaCO3)×$\frac{12}{100}$×100%
则m(CaCO3)=60g.
故答案为:A.
点评 解答本题的关键是元素守恒,要知道碳酸钙中碳元素的质量来自于一氧化碳和二氧化碳中的碳元素,再根据所提供的信息进行进一步计算.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
13.下列关于资源的叙述正确的是( )
| A. | 石油分馏可得到汽油、柴油等多种产品,是可再生能源 | |
| B. | 地球表面被四分之三水覆盖着,所以不必节约用水 | |
| C. | 空气是一种重要的自然资源,它是由氧气和氮气两种气体组成的 | |
| D. | 金属的回收利用不仅可以节约金属资源和能源,还可以减少对环境的污染 |
17.下列变化过程中,发生物理变化的是( )
| A. | 葡萄酿酒 | B. | 榨取果汁 | C. | 米饭变馊 | D. | 蛋清受热凝固 |
14.化学科学的发展促进了人类社会文明的进步,化学已日益渗透到社会生活的各个方面.你认为下列各项不属于化学学科研究范畴的是( )
| A. | 将废旧塑料变成汽车燃料 | B. | 研制新型航空材料 | ||
| C. | 研究地壳板块结构及运动规律 | D. | 研制新药 |

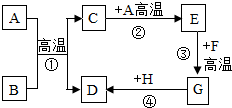 初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,H为蓝色溶液.它们的转化关系如图所示.请回答:
初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,H为蓝色溶液.它们的转化关系如图所示.请回答: 甲、乙、丙三种物质的溶解度曲线如图所示.据图回答:
甲、乙、丙三种物质的溶解度曲线如图所示.据图回答: