题目内容
 某同学使用图所示装置完成一氧化碳与氧化铁的反应.请回答下列有关问题:
某同学使用图所示装置完成一氧化碳与氧化铁的反应.请回答下列有关问题:(1)有下列实验步骤:①加热;②通入一氧化碳.实验开始时,应先进行的实验操作步骤的标号
(2)实验进行一段时间后,A装置中出现的现象为
考点:一氧化碳还原氧化铁,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)根据一氧化碳的可燃性分析实验步骤;
(2)根据实验原理分析实验现象及产物.
(2)根据实验原理分析实验现象及产物.
解答:解:(1)一氧化碳具有可燃性,点燃一氧化碳和空气或氧气的混合气体可能会发生爆炸,因此实验开始要先通入一氧化碳,排净玻璃管内的空气,防止加热时发生爆炸.然后再点燃酒精灯加热;
(2)一氧化碳与氧化铁反应生成铁和二氧化碳,因此A装置中可看到红棕色固体变黑,二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀,看到澄清石灰水变浑浊.
故答案为:(1)②;(2)红棕色固体变黑;3CO+Fe2O3
2Fe+3CO2;澄清石灰水变浑浊;CO2+Ca(OH)2=CaCO3↓+H2O.
(2)一氧化碳与氧化铁反应生成铁和二氧化碳,因此A装置中可看到红棕色固体变黑,二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀,看到澄清石灰水变浑浊.
故答案为:(1)②;(2)红棕色固体变黑;3CO+Fe2O3
| ||
点评:主要考查了一氧化碳的化学性质.要掌握一氧化碳还原氧化铁的实验中的现象和注意事项,并会根据反应现象寻出本质,

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
“绿色化学”是当今社会提出的一个新概念.在“绿色化学工艺”中,理想状态是反应中原子全部转化为欲制得的产物,即原子的利用率为100%.在用C3H4(丙炔)合成C5H8O2(2-甲基丙烯酸甲酯)的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要的其他反应物是( )
| A、CO和CH3OH |
| B、CO2和H2O |
| C、CO和C2H5OH |
| D、CH3OH和H2 |

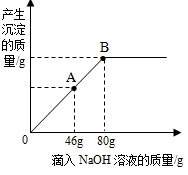 向盛有102g不饱和硫酸镁溶液的烧杯中,逐滴滴入溶质质量分数为10%的NaOH溶掖,产生沉淀的质量与所滴入NaOH溶液的质量关系曲线如图所示,请根据题意回答下列问题:
向盛有102g不饱和硫酸镁溶液的烧杯中,逐滴滴入溶质质量分数为10%的NaOH溶掖,产生沉淀的质量与所滴入NaOH溶液的质量关系曲线如图所示,请根据题意回答下列问题: 指出如图制取二氧化碳气体错误之处,并改正:
指出如图制取二氧化碳气体错误之处,并改正: