题目内容
11.小华在一次探究实验中将一小粒金属钠投入盛有蒸馏水的烧杯中,发现反应剧烈并生成大量可燃性气体,则该气体可能是( )| A. | H2 | B. | CH4 | C. | He | D. | CO |
分析 根据质量守恒定律,反应前后,元素种类不变,结合题意进行分析解答.
解答 解:根据质量守恒定律,反应物为钠和水,反应前有三种元素,即钠元素、氢元素和氧元素,反应后不会出现除这三种元素以外的其它元素.
A、反应物中含有氢元素,由反应前后元素种类不变,该气体可能是氢气,故选项正确.
B、反应物中不含碳元素,由反应前后元素种类不变,该气体不可能是CH4,故选项错误.
C、反应物中不含氦元素,由反应前后元素种类不变,该气体不可能是He,故选项错误.
D、反应物中不含碳元素,由反应前后元素种类不变,该气体不可能是一氧化碳,故选项错误.
故选:A.
点评 本题难度不大,掌握质量守恒定律(反应前后,元素种类不变)并能灵活运用是正确解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.除去下列物质中的杂质,所选用的试剂和操作方法都正确的是( )
| 选项 | 物质 | 杂质(少量) | 试剂及操作方法 |
| A | 铁 | 硫酸铜 | 加入足量水,过滤,洗涤,干燥 |
| B | 碘 | 高锰酸钾 | 加入足量水溶解,过滤,洗涤,干燥 |
| C | 硝酸亚铁溶液 | 硝酸银 | 加入足量的锌,过滤,蒸发,结晶 |
| D | 锌粉 | 铜 | 加入足量的稀盐酸,过滤,洗涤,干燥, |
| A. | A | B. | B | C. | C | D. | D |
2.在下列变化中,属于氧化反应但不属于化合反应的是( )
| A. | 碳+氧气$\stackrel{点燃}{→}$二氧化碳 | B. | 酒精+氧气$\stackrel{点燃}{→}$二氧化碳+水 | ||
| C. | 氧化汞$\stackrel{加热}{→}$汞+氧气 | D. | 镁+氧气$\stackrel{点燃}{→}$氧化镁 |
19. 钢铁工业是国家工业的基础.
钢铁工业是国家工业的基础.
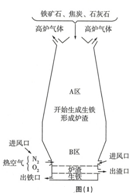
(1)如图(1)是炼铁高炉及炉内化学变化过程示意图.
根据图示回答下列问题.
若图中采用的铁矿石的主要成分为氧化铁,请写出A区和B区所发生主要反应的化学方程式:
A区Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
B区C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
(2)某兴趣小组利用图(2)实验装置测定某赤铁矿石样品中Fe2O3的质量分数,取10g样品与足量CO充分反应后,测得剩余固体的质量为7.6g,下列说法正确的是D(温馨提示:杂质不参加反应)
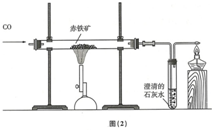
A.玻璃管中的固体由黑色逐渐变成红色
B.实验中通入CO的质量为4.2g
C.生成CO2的质量为2.4g
D.铁矿石样品中Fe2O3的质量分数为80%
(3)小组同学又用一氧化碳还原纯净的氧化铁粉末,同时对固体产物的成分进行探究.
该小组按图(3)实验设计,在一定温度下进行了实验,测得下列数据:
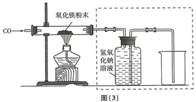
①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g)
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却至室温称量)
【分析与讨论】
本实验中,玻璃管内固体粉末由红色全部变为黑色.小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,她质疑的理由是如果黑色固体全部是铁,则质量应该为:6.0g×70%=4.2g,不应该是5.8g.于是大家提出查阅资料.
【查阅资料】
①一氧化碳还原氧化铁的固体产物的成分与反应温度、反应时间等因素有关.
②一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁
③
【实验与猜想】
①该小组的同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和氧化亚铁.
②进行猜想:黑色固体粉末可能是
a.四氧化三铁 b.四氧化三铁和铁
【得出结论】
通过实验中获得的数据进行计算,得出黑色固体粉末为四氧化三铁(写名称).
【反思与评价】
①一氧化碳还原氧化铁的实验中,若要得到铁可适当提高反应温度和延长反应时间.
②实验装置图(3)中采用虚线框内的装置,其作用有AB.
A.收集一氧化碳 B.吸收二氧化碳 C.检验二氧化碳.
③工业上炼出的生铁与实验还原出来的铁有什么区别?工业上炼出的生铁中含有碳,而实验还原出来的铁中不含有碳.将工业上炼出的生铁少量放于烧杯中,加入足量稀盐酸的现象是固体部分溶解,产生气泡,溶液变成浅绿色.
 钢铁工业是国家工业的基础.
钢铁工业是国家工业的基础.(1)如图(1)是炼铁高炉及炉内化学变化过程示意图.
根据图示回答下列问题.
若图中采用的铁矿石的主要成分为氧化铁,请写出A区和B区所发生主要反应的化学方程式:
A区Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
B区C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
(2)某兴趣小组利用图(2)实验装置测定某赤铁矿石样品中Fe2O3的质量分数,取10g样品与足量CO充分反应后,测得剩余固体的质量为7.6g,下列说法正确的是D(温馨提示:杂质不参加反应)

A.玻璃管中的固体由黑色逐渐变成红色
B.实验中通入CO的质量为4.2g
C.生成CO2的质量为2.4g
D.铁矿石样品中Fe2O3的质量分数为80%
(3)小组同学又用一氧化碳还原纯净的氧化铁粉末,同时对固体产物的成分进行探究.
该小组按图(3)实验设计,在一定温度下进行了实验,测得下列数据:

①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g)
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却至室温称量)
【分析与讨论】
本实验中,玻璃管内固体粉末由红色全部变为黑色.小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,她质疑的理由是如果黑色固体全部是铁,则质量应该为:6.0g×70%=4.2g,不应该是5.8g.于是大家提出查阅资料.
【查阅资料】
①一氧化碳还原氧化铁的固体产物的成分与反应温度、反应时间等因素有关.
②一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁
③
| 物质 性质 | 四氧化三铁 | 氧化亚铁 | 氧化铁 | 铁粉 |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
①该小组的同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和氧化亚铁.
②进行猜想:黑色固体粉末可能是
a.四氧化三铁 b.四氧化三铁和铁
【得出结论】
通过实验中获得的数据进行计算,得出黑色固体粉末为四氧化三铁(写名称).
【反思与评价】
①一氧化碳还原氧化铁的实验中,若要得到铁可适当提高反应温度和延长反应时间.
②实验装置图(3)中采用虚线框内的装置,其作用有AB.
A.收集一氧化碳 B.吸收二氧化碳 C.检验二氧化碳.
③工业上炼出的生铁与实验还原出来的铁有什么区别?工业上炼出的生铁中含有碳,而实验还原出来的铁中不含有碳.将工业上炼出的生铁少量放于烧杯中,加入足量稀盐酸的现象是固体部分溶解,产生气泡,溶液变成浅绿色.
6.2014年5月29日《环球时报》报道:我国科学家率先用铝合金和石墨烯(一种碳单质)按一定比例混合制成“烯合金”,该材料有望生产出“纸一样薄的手机”、“一分钟充满电的电池”等产品.下列关于“烯合金”的说法中一定不正确的是( )
| A. | 是一种混合物 | B. | 具有导电性 | C. | 不与酸反应 | D. | 具有可燃性 |
20.在化学反应2A+B=2C中,设有6克A和B完全反应生成14克的C,若B的相对分子质量是32,则c 的相对分子质量为( )
| A. | 56 | B. | 28 | C. | 20 | D. | 44 |
1.下列关于物质的组成和构成的说法中正确的是( )
| A. | 物质都是由多种元素组成 | B. | 含有不同元素的物质一定是化合物 | ||
| C. | 任何物质都是由一种元素组成 | D. | 物质并不都是由分子构成的 |
 某兴趣小组的同学用右图所示的装置测定空气中氧气的含量,先在瓶中装入少量某液体X,并将液面以上的空间分为5等份,实验结束,他们观察到瓶内液面到达图中“1”刻度处,且量筒中的水减少了44.8ml.
某兴趣小组的同学用右图所示的装置测定空气中氧气的含量,先在瓶中装入少量某液体X,并将液面以上的空间分为5等份,实验结束,他们观察到瓶内液面到达图中“1”刻度处,且量筒中的水减少了44.8ml.