题目内容
19. 钢铁工业是国家工业的基础.
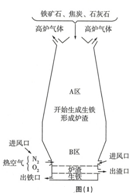
钢铁工业是国家工业的基础.(1)如图(1)是炼铁高炉及炉内化学变化过程示意图.
根据图示回答下列问题.
若图中采用的铁矿石的主要成分为氧化铁,请写出A区和B区所发生主要反应的化学方程式:
A区Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
B区C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
(2)某兴趣小组利用图(2)实验装置测定某赤铁矿石样品中Fe2O3的质量分数,取10g样品与足量CO充分反应后,测得剩余固体的质量为7.6g,下列说法正确的是D(温馨提示:杂质不参加反应)
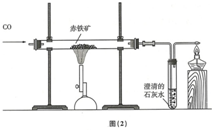
A.玻璃管中的固体由黑色逐渐变成红色
B.实验中通入CO的质量为4.2g
C.生成CO2的质量为2.4g
D.铁矿石样品中Fe2O3的质量分数为80%
(3)小组同学又用一氧化碳还原纯净的氧化铁粉末,同时对固体产物的成分进行探究.
该小组按图(3)实验设计,在一定温度下进行了实验,测得下列数据:
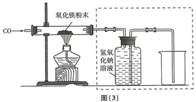
①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g)
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却至室温称量)
【分析与讨论】
本实验中,玻璃管内固体粉末由红色全部变为黑色.小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,她质疑的理由是如果黑色固体全部是铁,则质量应该为:6.0g×70%=4.2g,不应该是5.8g.于是大家提出查阅资料.
【查阅资料】
①一氧化碳还原氧化铁的固体产物的成分与反应温度、反应时间等因素有关.
②一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁
③
| 物质 性质 | 四氧化三铁 | 氧化亚铁 | 氧化铁 | 铁粉 |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
①该小组的同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和氧化亚铁.
②进行猜想:黑色固体粉末可能是
a.四氧化三铁 b.四氧化三铁和铁
【得出结论】
通过实验中获得的数据进行计算,得出黑色固体粉末为四氧化三铁(写名称).
【反思与评价】
①一氧化碳还原氧化铁的实验中,若要得到铁可适当提高反应温度和延长反应时间.
②实验装置图(3)中采用虚线框内的装置,其作用有AB.
A.收集一氧化碳 B.吸收二氧化碳 C.检验二氧化碳.
③工业上炼出的生铁与实验还原出来的铁有什么区别?工业上炼出的生铁中含有碳,而实验还原出来的铁中不含有碳.将工业上炼出的生铁少量放于烧杯中,加入足量稀盐酸的现象是固体部分溶解,产生气泡,溶液变成浅绿色.
分析 (1)高温条件下,氧化铁和一氧化碳反应生成铁和二氧化碳;
碳燃烧生成二氧化碳,二氧化碳在高温条件下和碳反应生成一氧化碳;
(2)为了防止发生爆炸,加热前应该先通入一会儿一氧化碳,反应结束后,应该继续通入一氧化碳直至玻璃管冷却至室温;
(3)氢氧化钠溶液能够吸收二氧化碳;
氧化铁中铁元素质量分数=$\frac{112}{160}$×100%=70%;
根据实验现象可以判断相关方面的问题;
铁和稀盐酸反应生成氯化亚铁和氢气.
解答 解:(1)A区中,氧化铁和一氧化碳反应生成铁和二氧化碳,反应的化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
B区中,碳燃烧生成二氧化碳,二氧化碳和碳反应生成一氧化碳,反应的化学方程式分别为:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
(2)A.应该是玻璃管中的固体由红色逐渐变成黑色,该选项说法不正确;
B.取10g样品与足量CO充分反应后,测得剩余固体的质量为7.6g,说明氧化铁中氧元素质量为:10g-7.6g=2.4g,则氧化铁质量为:2.4g÷30%=8g,
设反应需要一氧化碳质量为x,生成二氧化碳质量为y,
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,
160 84 132
8g x y
$\frac{160}{8g}$=$\frac{84}{x}$=$\frac{132}{y}$,
x=4.1g,y=6.6g,
因为反应前后要通入一氧化碳,因此实验中通入CO的质量应该大于4.2g,该选项说法不正确;
C.生成CO2的质量是6.6g,该选项说法不正确;
D.铁矿石样品中Fe2O3的质量分数为:$\frac{8g}{10g}$×100%=80%,该选项说法正确.
故填:D.
(3)【分析与讨论】
她质疑的理由是如果黑色固体全部是铁,则质量应该为:6.0g×70%=4.2g,不应该是5.8g.
故填:如果黑色固体全部是铁,则质量应该为:6.0g×70%=4.2g,不应该是5.8g.
【实验与猜想】
①该小组的同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和氧化亚铁.
故填:氧化亚铁.
②黑色固体粉末可能是四氧化三铁,或四氧化三铁和铁.
故填:四氧化三铁;四氧化三铁和铁.
【得出结论】
假设产物是四氧化三铁,生成四氧化三铁质量为z,
3Fe2O3+CO$\frac{\underline{\;高温\;}}{\;}$2Fe3O4+3CO2,
480 464
6.0g z
$\frac{480}{6.0g}$=$\frac{464}{z}$,
z=5.8g,
与假设符合,因此通过实验中获得的数据进行计算,得出黑色固体粉末为四氧化三铁.
故填:四氧化三铁.
【反思与评价】
②实验装置图(3)中采用虚线框内的装置,其作用有收集一氧化碳,吸收二氧化碳.
故填:AB.
③工业上炼出的生铁与实验还原出来的铁的区别是:工业上炼出的生铁中含有碳,而实验还原出来的铁中不含有碳;
将工业上炼出的生铁少量放于烧杯中,加入足量稀盐酸的现象是固体部分溶解,产生气泡,溶液变成浅绿色.
故填:工业上炼出的生铁中含有碳,而实验还原出来的铁中不含有碳;固体部分溶解,产生气泡,溶液变成浅绿色.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案①制铝锭 ②制易拉罐 ③制电线电缆 ④制牙膏皮 ⑤用明矾净水 ⑥制炊具 ⑦用明矾和苏打作食品膨化剂 ⑧用氢氧化铝制胃药 ⑨制防锈油漆.
| A. | ①②④⑤⑥⑦⑧ | B. | ②④⑤⑥⑦⑧ | C. | ②⑤⑥⑦⑧ | D. | ③④⑤⑥⑦⑧ |
| A. | 水 | B. | 铁 | C. | 汞 | D. | 氯化钠 |
【实验过程】
甲组实验方案:将四瓶溶液标号分别为1、2、3、4,只利用紫色石蕊溶液进行实验.

乙组实验方案:不用其他试剂进行实验.
| 实验操作 | 实验现象 | 实验结论 |
| 任取三种溶液于三支试管中,分别滴加第四种溶液 | ①一支试管中有气泡放出,其余两支试管中无明显变化 | ①第四种溶液为稀盐酸 |
| ②一支试管中有白色沉淀析出,其余两支试管中溶液无明显变化 | ③第四种为Na2CO3溶液 | |
| ④三支试管中溶液均无明显变化 | ②第四种为NaOH溶液 |
经过交流后,发现实验结论②(填序号)是不正确的;若该结论作正确,对应的实验现象应是一支试管中有气泡放出、一支试管中有白色沉淀析出、一支试管中无明显现象.
丙组实验方案:将四种溶液编号为1、2、3、4,不用其他试剂进行实验.

丁组实验方案:将四种溶液重新编号为1、2、3、4,各取少量溶液于四支试管中,分别加热.1中产生刺激性气味,2、3无明显变化,4中溶液变浑浊.冷却后,再取少量澄清4号溶液滴入2、3中,2号溶液无明显变化,3号溶液变浑浊.
通过以上实验,鉴别出号溶液是稀盐酸;加热4号溶液变浑浊的原因是氢氧化钙的溶解度随温度的升高而降低,因此石灰水加热时会有氢氧化钙的析出.
| A. | H2 | B. | CH4 | C. | He | D. | CO |
 .
.