题目内容
6.一包白色分粉末,由硫酸铜、碳酸钠、氯化钡、硫酸钠、氢氧化钠、氯化钠中的两种或两种以上的物质混合而成.为了探究其组成,进行了如下实验:(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到沉淀和无色滤液.则原白色粉末中是否含有硫酸铜?答:不确定(填“有”、“没有”、“不能确定”)
(2)取实验(1)滤出的沉淀,向其中加入足量的稀盐酸,产生无色气体,沉淀全部溶解形成无色溶液,则原白色粉末中的组成有4种可能.
(3)小益想探究原白色粉末中是否含有氢氧化钠固体,他设计了如下的实验操作:
①取(1)中少量无色滤液,向其中滴入氯化钡溶液,有白色沉淀生成.
②继续滴加氯化钡溶液至不再产生沉淀为止
③向上清液中滴加酚酞.
分析 根据硫酸铜在溶液中显蓝色,硫酸铜和氢氧化钠会生成蓝色氢氧化铜沉淀和硫酸钠,碳酸钠和氯化钡会生成溶于酸的碳酸钡沉淀,硫酸钠和氯化钡会生成不溶于酸的硫酸钡沉淀等知识进行分析.
解答 解:(1)硫酸铜在溶液中显蓝色,硫酸铜和氢氧化钠会生成蓝色氢氧化铜沉淀和硫酸钠,取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到沉淀和无色滤液,没有说明沉淀的颜色,所以不能确定原白色粉末中是否含有硫酸铜;
(2)取实验(1)滤出的沉淀,向其中加入足量的稀盐酸,产生无色气体,沉淀全部溶解形成无色溶液,所以沉淀中一定不含氢氧化铜沉淀,原混合物中一定不含硫酸铜,一定含有碳酸钠、氯化钡,可能含有氢氧化钠、氯化钠,所以原白色粉末中的组成是:碳酸钠、氯化钡、氢氧化钠,碳酸钠、氯化钡、氯化钠,碳酸钠、氯化钡、氢氧化钠、氯化钠4种可能;
(3)药用酚酞检验氢氧化钠,需要加入氯化钡除去碳酸钠,所以
①取(1)中少量无色滤液,向其中滴入氯化钡溶液,有白色沉淀生成;
②继续滴加氯化钡溶液至不再产生沉淀为止;
③向上清液中滴加酚酞,酚酞变红,证明含有氢氧化钠.
故答案为:(1)不确定;
(2)4;
(3)继续滴加氯化钡溶液至不再产生沉淀为止;向上清液中滴加酚酞.
点评 在解此类题时,首先分析题中所给物质的性质,然后依据题中的现象确定各种物质的存在性,最后确定混合物的成分.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.消防队用水灭火主要是因为( )
| A. | 水不能燃烧也不支持燃烧 | B. | 降低可燃物的温度低于着火点 | ||
| C. | 降低可燃物的着火点 | D. | 上述A与C的双重作用 |
 以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图.如图所示为铁的价类图.例如E点可表示+2价的亚铁盐.请回答:
以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图.如图所示为铁的价类图.例如E点可表示+2价的亚铁盐.请回答: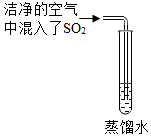 雨、雪在形成和降落过程中吸收、溶解了空气中SO2、及氮氧化物等物质,形成了pH小于5.6的降水称为酸雨,请回答下列有关酸雨的问题:
雨、雪在形成和降落过程中吸收、溶解了空气中SO2、及氮氧化物等物质,形成了pH小于5.6的降水称为酸雨,请回答下列有关酸雨的问题:
 在萧山区实验创新比赛中,某教师用饮料瓶代替吸滤瓶,并用玻璃棒将试管顶住,如图所示,实验现象非常明显且灭火效果很好.实验步骤如下:
在萧山区实验创新比赛中,某教师用饮料瓶代替吸滤瓶,并用玻璃棒将试管顶住,如图所示,实验现象非常明显且灭火效果很好.实验步骤如下: