题目内容
12. 研究金属活动性强弱,对合理利用金属资源有着重要意义.同学们通过以下活动进行了铁、铝、铜三种金属活动下的研究,都得到了正确的结论:
研究金属活动性强弱,对合理利用金属资源有着重要意义.同学们通过以下活动进行了铁、铝、铜三种金属活动下的研究,都得到了正确的结论:【活动研究】方案一 查阅资料得知,在原始社会末期就有了青铜器,约2500年前开始生产和使用铁器.
约200多年前才开始使用铝制品,由此推出三种金属的活动性由强到弱的顺序是铝、铁、铜.
方案二 把等面积足量的三种金属薄片放入三支试管中,分别加入等质量等浓度的稀盐酸,观察到的现象是铝片上产生气泡速率快,铁片上产生气泡速率慢,铜片上不产生气泡,同时得到如图曲线,其中铝与稀盐酸的反应过程应是图中的a(填“a”或“b”).
方案三 同学们运用金属与盐的反应也可以证明三种金属的活动性顺序,他们所选的试剂有硫酸铝溶液、铁、硫酸铜溶液,该方案中的化学方程式为Fe+CuSO4═FeSO4+Cu.
【反思与质疑】生活中我们常常看到铁制品易生锈,而铝制品不易生锈,小明同学认为铁比铝活泼,你的观点和理由是铝比铁活泼,铝制品不易生锈,是因为通常情况下铝能和空气中的氧气反应生成一次致密的氧化物薄膜,对铝制品起到了保护作用.
分析 金属被发现和使用的越早,化学性质越不活泼;
铝和稀盐酸反应生成氯化铝和氢气,铁和稀盐酸反应生成氯化亚铁和氢气,铜不能和稀盐酸反应;
铁和硫酸铜反应生成硫酸亚铁和铜;
通常情况下,铝能和空气中的氧气反应生成氧化铝,氧化铝能够对铝起到保护作用.
解答 解:【活动研究】
在原始社会末期就有了青铜器,约2500年前开始生产和使用铁器,约200多年前才开始使用铝制品,由此推出三种金属的活动性由强到弱的顺序是铝、铁、铜.
故填:铝、铁、铜.
把等面积足量的三种金属薄片放入三支试管中,分别加入等质量等浓度的稀盐酸,观察到的现象是铝片上产生气泡速率快,铁片上产生气泡速率慢,铜片上不产生气泡;
同时得到如图曲线,其中铝与稀盐酸的反应过程应是图中的a,这是因为铝比铁活泼,反应需要的时间短.
故填:铝片上产生气泡速率快,铁片上产生气泡速率慢,铜片上不产生气泡;a.
同学们运用金属与盐的反应也可以证明三种金属的活动性顺序,他们所选的试剂可以是硫酸铝溶液、铁、硫酸铜溶液,把铁丝伸入硫酸铝溶液中时,无明显现象,说明铁不如铝活泼,把铁丝伸入硫酸铜溶液中时,铁丝表面附着了一层红色固体,说明铁比铜活泼,铁和硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu.
故填:硫酸铝溶液、铁、硫酸铜溶液;Fe+CuSO4═FeSO4+Cu.
【反思与质疑】
生活中我们常常看到铁制品易生锈,而铝制品不易生锈,小明同学认为铁比铝活泼,你的观点和理由是:铝比铁活泼,铝制品不易生锈,是因为通常情况下铝能和空气中的氧气反应生成一次致密的氧化物薄膜,对铝制品起到了保护作用.
故填:铝比铁活泼,铝制品不易生锈,是因为通常情况下铝能和空气中的氧气反应生成一次致密的氧化物薄膜,对铝制品起到了保护作用.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案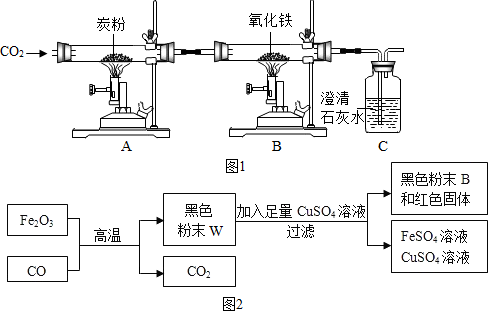
(1)写出装置A玻璃管中发生反应的化学方程式:C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO;
(2)整套装置还有一个明显的不足之处是:缺少尾气处理装置.
(3)B中得到的黑色产物W,该活动小组同学根据图2对产物W的成分进行探究.
【提出问题】黑色粉末W可能是什么呢?
【查阅资料】
①铁的氧化物有氧化铁,氧化亚铁和四氧化三铁等,其中氧化铁为红棕色,其余都为黑色.
②铁的氧化物中四氧化三铁有磁性,能被磁铁吸引.
③铁的氧化物都难溶于水,却都能与稀盐酸反应而被溶解.
④铁的氧化物通常情况下不与CuSO4溶液反应.
【进行猜想】
①甲同学认为黑色粉末W全部是铁粉.请写出生成铁的化学反应方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.该反应利用了CO的还原性.
②乙同学认为甲同学的猜想是错误的,理由是黑色粉末W与足量的硫酸铜溶液反应后仍有黑色固体存在.
③丙同学认为黑色粉末W中不含Fe2O3,理由是氧化铁是红棕色的固体.
丙同学提出如下猜想,请你结合所学知识帮他补充完整.
猜想1:黑色粉末W由铁粉和四氧化三铁(Fe2O3)组成;
猜想2:黑色粉末W由铁粉和氧化亚铁(FeO)组成;
猜想3:黑色粉末W由铁粉、四氧化三铁(Fe2O3)、氧化亚铁(FeO).
【实验探究】
| 方案 | 实验操作 | 可能的现象 | 结论 |
| ① | 取适量黑色粉末W用磁铁吸引 | 黑色粉末全部被吸引 | 猜想1正确 |
| ② | 取适量黑色粉末W用磁铁吸引 | 黑色粉末部分被吸引 | 猜想2正确 |
| ③ | 取适量黑色粉末R用加入足量稀盐酸 | 黑色粉末全部溶解 | 猜想3正确 |
| ④ | 取适量黑色粉末R用磁铁吸引 | 黑色固体部分被吸引 | 猜想4正确 |
【反思提高】
丁同学认为方案②和方案③中得出的结论不正确,其理由是若有四氧化三铁(Fe3O4)存在,现象相同(或者不能证明没有四氧化三铁(Fe3O4),合理即可).
查阅资料知道:
Fe3O4溶于稀盐酸生成FeCl3、FeCl2和水,其反应方程式可表示为Fe3O4+8HCl=2FeCl3+FeCl2+4H2O
Fe3O4也能溶于稀硝酸(HNO3),反应生成Fe(NO3)3、NO和水,试写出反应的化学方程式3Fe3O4+28HNO3=9Fe(NO3)3+NO+14H2O.
| 序号 | 待鉴别的物质 | 鉴别试剂或方法 |
| A | 氧化铜与氧化铁 | 观察颜色 |
| B | 硝酸铵与食盐固体 | 水 |
| C | 氢氧化钠溶液与碳酸钠溶液 | 酚酞溶液 |
| D | 氧气与二氧化碳 | 带火星的木条 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 30.4g | B. | 28 g | C. | 35.6g | D. | 29.8g |
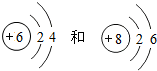 两种原子中相等的是( )
两种原子中相等的是( )| A. | 质子数 | B. | 电子数 | C. | 第一层电子数 | D. | 第二层电子数 |
