题目内容
20.工业上煅烧石灰石反应一段时间后,小附同学取32g反应后的剩余物,加入200g质量分数为14.6%的稀盐酸恰好完全反应,测得反应后液体的质量为222.4g,得滤渣5.2g,则此剩余物中钙元素的质量分数为( )| A. | 50% | B. | 80% | C. | 12.5% | D. | 20% |
分析 石灰石高温锻烧,碳酸钙分解生成氧化钙和二氧化碳,锻烧后固体与盐酸反应,碳酸钙与盐酸反应生成氯化钙、水、二氧化碳而氧化钙与盐酸生成氯化钙和水,因此,反应后所得溶液一定是氯化钙,其中钙元素质量即石灰石中碳酸钙中钙元素的质量、氯元素质量即所加盐酸中氯元素质量;利用氯化钙中氯元素与钙元素质量关系,可由盐酸中所含氯元素质量求得碳酸钙中钙元素质量,最终根据题意完成原石灰石样品中钙的质量分数的计算.
解答 解:200g质量分数为14.6%的稀盐酸中所含氯元素质量=200g×14.6%×$\frac{35.5}{36.5}$×100%=28.4g
氯化钙中钙元素与氯元素质量比=40:(35.5×2)=40:71,则氯化钙中氯元素质量为28.4g时钙元素质量=$\frac{28.4g}{71}$×40=16g
则原石灰石样品中钙的质量分数=$\frac{16g}{32g}$×100%=50%
故选:A
点评 根据化学变化前后元素质量不变,通过氯化钙中氯元素与钙元素质量关系,这是解答本题的技巧所在.

练习册系列答案
相关题目
10.水电解产生氢气和氧气,则化学计量数之比:ν(H2):ν(O2)等于( )
| A. | 1:1 | B. | 2:1 | C. | 2:32 | D. | 4:32 |
11.将硫酸渣中金属元素进行分离的一种工艺流程如图所示

【查阅资料】
Ⅰ.相关数据
Ⅱ.25℃时,Al(OH)3可溶于pH>6.0的碱溶液,并转化为AlO2-
【流程分析】
(1)在实验室完成操作①需要的玻璃仪器有烧杯、玻璃棒和漏斗
(2)所加稀盐酸必须过量的原因是使硫酸渣完全溶解
(3)向溶液A中加入试剂M调节pH到7的过程中,沉淀的颜色会经历“红褐色变淡,再变深”的过程,出现该现象的原因是氢氧化钠会与氯化铁反应生成氢氧化铁沉淀,氢氧化铁沉淀会溶于酸,盐酸消耗完后,氢氧化铁沉淀的沉淀量会逐渐增多,颜色变深
(4)溶液B中加入试剂M调节pH=13时,发生反应的化学方程式是AlCl3+4NaOH=NaAlO2+2H2O+3NaCl,MgCl2+2NaOH=Mg(OH)2↓+2NaCl
(5)高温灼烧固体X时,X能在保持各元素化合价不变的前提下分解为两种氧化物,该反应的化学方程式是2Fe(OH)3$\frac{\underline{\;高温\;}}{\;}$Fe2O3+3H2O
(6)如果操作②是蒸发结晶,则不可能得到纯净的NaAlO2固体,理由是:溶液C中含有反应生成的氯化钠.

【查阅资料】
Ⅰ.相关数据
| 25℃时,氢氧化钠沉淀的pH范围 | |||
| Fe(OH)3 | Al(OH)3 | Mg(OH)2 | |
| 开始沉淀的pH | 1.5 | 3.3 | 10.4 |
| 沉淀完全的pH | 3.2 | 5.2 | 12.4 |
【流程分析】
(1)在实验室完成操作①需要的玻璃仪器有烧杯、玻璃棒和漏斗
(2)所加稀盐酸必须过量的原因是使硫酸渣完全溶解
(3)向溶液A中加入试剂M调节pH到7的过程中,沉淀的颜色会经历“红褐色变淡,再变深”的过程,出现该现象的原因是氢氧化钠会与氯化铁反应生成氢氧化铁沉淀,氢氧化铁沉淀会溶于酸,盐酸消耗完后,氢氧化铁沉淀的沉淀量会逐渐增多,颜色变深
(4)溶液B中加入试剂M调节pH=13时,发生反应的化学方程式是AlCl3+4NaOH=NaAlO2+2H2O+3NaCl,MgCl2+2NaOH=Mg(OH)2↓+2NaCl
(5)高温灼烧固体X时,X能在保持各元素化合价不变的前提下分解为两种氧化物,该反应的化学方程式是2Fe(OH)3$\frac{\underline{\;高温\;}}{\;}$Fe2O3+3H2O
(6)如果操作②是蒸发结晶,则不可能得到纯净的NaAlO2固体,理由是:溶液C中含有反应生成的氯化钠.
15.取石灰石样品16g,把80g稀盐酸分四次加入,实验过程所得数据如下表(已知石灰石样品中含有的二氧化硅等杂质不溶于水,不与稀盐酸反应).根据实验数据计算:
(1)表中 n的数值为2.8.
(2)样品中碳酸钙的质量分数是82.5%.
(3)求反应结束时生成二氧化碳的质量.
| 实验次数 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
| 1 | 20 | 11 |
| 2 | 20 | 6 |
| 3 | 20 | 2.8 |
| 4 | 20 | n |
(2)样品中碳酸钙的质量分数是82.5%.
(3)求反应结束时生成二氧化碳的质量.
5.写出下列符号(或名称)
| 名称 | 锂 | 氢 | 磷 | 镁 | 铝 | 锌 | |
| 元素符号 | Ca | ||||||
| 名称 | 氮 | 钾 | 氯 | 氩 | 铁 | ||
| 元素符号 | S | Na |
12.加热10g高锰酸钾一段时间后,停止加热,称量剩余固体的质量为9.2g.那么剩余固体的成分是( )
| A. | K2MnO4、MnO2 | B. | KMnO4、MnO2 | ||
| C. | KMnO4、K2MnO4、MnO2 | D. | KMnO4、K2MnO4 |
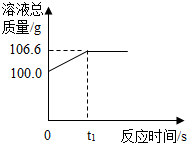 为测定某赤铁矿石中氧化铁的质量分数,小龙和他的同学用足量的一氧化碳与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用一定量的氢氧化钠溶液完全吸收,该溶液总质量与反应时间的变化关系如图.
为测定某赤铁矿石中氧化铁的质量分数,小龙和他的同学用足量的一氧化碳与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用一定量的氢氧化钠溶液完全吸收,该溶液总质量与反应时间的变化关系如图. 小李对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.请填写下列空格:
小李对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.请填写下列空格: