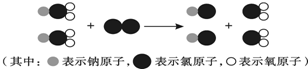
题目内容
16.点燃密闭容器中的10g氢气和氧气的混合气体,爆炸后冷却,剩余1g氧气,则混合气体的组成可能是( )| A. | 2gH2,8gO2 | B. | 1g H2,9g O2 | C. | 4gH2,5gO2 | D. | 5gH2,5gO2 |
分析 根据氢气在氧气中燃烧的化学方程式,由生成水的质量,计算出参加反应的氢气和氧气的质量,进行分析解答即可
解答 解:点燃密闭容器中的10g氢气和氧气的混合气体,爆炸后冷却,剩余1g氧气,则参加反应的氢气和氧气的质量之和为10g-1g=9g,由质量守恒定律,生成水的质量为9g.
设参加反应的氢气的质量为x,
2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O
4 36
x 9g
$\frac{4}{36}=\frac{x}{9g}$ x=1g
参加反应的氧气的质量为9g-1g=8g
反应后氧气有剩余,则反应前混合气体中含氧气为1g+8g=9g.
故选:B.
点评 本题难度不是很大,考查学生利用化学反应方程式的计算来分析混合物的成分,利用化学反应判断恰好完全反应的量是正确解题的关键.

练习册系列答案
相关题目
6.物质与水发生的复分解反应称为水解反应.例如:Al2S3+6H2O═2Al(OH)3↓+3H2S↑.根据上述观点,下列说法中不正确的是( )
| A. | NaF的水解产物是NaOH和HF | B. | CaO2的水解产物是Ca(OH)2和C2H2 | ||
| C. | PCl3的水解产物之一是PH3 | D. | Mg3N2水解产物是Mg(OH)2和NH3 |
8.某元素的化合物的化学式为R2O3,其中氧元素的质量百分含量为30%,则R的相对原子质量是( )
| A. | 27 | B. | 23 | C. | 39 | D. | 56 |
5.海湾战争引起科威特大量油井燃烧,造成严重的大气污染.据报导,有些地区降黑雨,你分析形成黑雨的主要污染成分是( )
| A. | 炭黑 | B. | 二氧化氮 | C. | 二氧化硫 | D. | 一氧化碳 |