题目内容
9.含锌废渣和各种锌矿(如菱锌矿)都有着重要的用途.以含锌废渣(主要成分为ZnO,杂质为FeO、CuO)为原料制备七水硫酸锌(ZnSO4•7H2O)的流程如图.

(1)粉碎的目的是增大反应物接触面积,加快反应速率.
(2)若实验室用质量分数为98%的硫酸配制200g 25%的硫酸,需要的玻璃仪器有胶头滴管、玻璃棒、烧杯和量筒,此处玻璃棒的作用是搅拌加快散热.
(3)物质X是锌,滤渣中含有金属单质有锌、铜,除铜时发生的反应方程式为Zn+CuSO4═ZnSO4+Cu.
(4)流程中获得七水硫酸锌前省略的操作是加热条件下制成硫酸锌的饱和溶液、冷却结晶、过滤、洗涤和低温烘干.
(5)某温度下,Fe(OH)3分解得到一种铁、氧质量比为21:8的氧化物,该氧化物的化学式是Fe3O4.
分析 (1)反应物接触面积越大,反应速率越快;
(2)浓硫酸溶于水放热;
(3)锌和硫酸铜反应生成硫酸锌和铜;
(4)可以通过降温方法得到硫酸锌晶体;
(5)根据铁元素和氧元素的质量比可以计算铁的氧化物的化学式.
解答 解:(1)粉碎的目的是增大反应物接触面积,加快反应速率.
故填:增大反应物接触面积,加快反应速率.
(2)若实验室用质量分数为98%的硫酸配制200g 25%的硫酸,需要的玻璃仪器有胶头滴管、玻璃棒、烧杯和量筒,此处玻璃棒的作用是搅拌加快散热.
故填:烧杯;量筒;搅拌加快散热.
(3)物质X是锌,锌能和硫酸铜反应生成硫酸锌和铜,可以把硫酸铜除去,滤渣中含有金属单质有过量的锌和反应生成的铜,除铜时发生的反应方程式为:Zn+CuSO4═ZnSO4+Cu.
故填:锌;锌、铜;Zn+CuSO4═ZnSO4+Cu.
(4)流程中获得七水硫酸锌前省略的操作是加热条件下制成硫酸锌的饱和溶液、冷却结晶、过滤、洗涤和低温烘干.
故填:加热条件下制成硫酸锌的饱和溶液;过滤.
(5)设铁的氧化物的化学式是FexOy,根据题意有:$\frac{56x}{16y}$=$\frac{21}{8}$,
$\frac{x}{y}$=$\frac{3}{4}$,
该氧化物的化学式是Fe3O4.
故填:Fe3O4.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案
相关题目
17.如图是氯元素在元素周期表中的信息和氯原子结构示意图.下列说法错误的是( )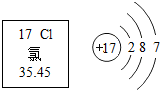

| A. | 氯的原子序数为17 | |
| B. | 氯原子核外有3个电子层 | |
| C. | 氯的相对原子质量为35.45 | |
| D. | 在化学反应中,氯原子容易失去最外层电子 |
4.如图为实验室常用的制取气体装置:
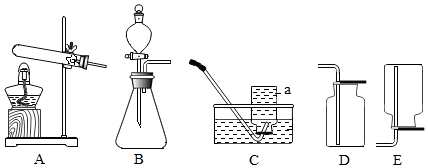
(1)仪器a的名称是集气瓶;组装A装置时,酒精灯应在固定试管之前(填“前”或“后”)放置.
(2)实验室用高锰酸钾制取氧气,反应的化学方程式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,宜选用的发生装置是A(填装置标号,下同),不宜选用的收集装置是E.
(3)实验室制取二氧化碳的研究中,在其他条件相同的情况下,进行如下实验:
①实验室制取二氧化碳的化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑.
②若要研究盐酸浓度大小对反应快慢的影响,可选择实验甲与乙(填实验编号)对照.
③除盐酸的浓度外,上述实验研究的另一个影响反应快慢的因素是固体反应物的颗粒大小(或反应物的接触面积).
④研究发现盐酸的浓度越大,产生气体越快.与甲比较,下列对丁分析正确的是A(填标号)
A.反应更剧烈 B.产生的二氧化碳的质量更大 C.参加反应的大理石更多
(4)请从实验原理、原料、发生装置、操作等方面,阐述下列实验中可以产生较平稳气体的主要原因.

(1)仪器a的名称是集气瓶;组装A装置时,酒精灯应在固定试管之前(填“前”或“后”)放置.
(2)实验室用高锰酸钾制取氧气,反应的化学方程式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,宜选用的发生装置是A(填装置标号,下同),不宜选用的收集装置是E.
(3)实验室制取二氧化碳的研究中,在其他条件相同的情况下,进行如下实验:
| 实验标号 药品 | 甲 | 乙 | 丙 | 丁 |
| 大理石(m0g) | 块状 | 块状 | 粉末状 | 粉末状 |
| 盐酸(过量) | 稀盐酸 | 浓盐酸 | 稀盐酸 | 浓盐酸 |
②若要研究盐酸浓度大小对反应快慢的影响,可选择实验甲与乙(填实验编号)对照.
③除盐酸的浓度外,上述实验研究的另一个影响反应快慢的因素是固体反应物的颗粒大小(或反应物的接触面积).
④研究发现盐酸的浓度越大,产生气体越快.与甲比较,下列对丁分析正确的是A(填标号)
A.反应更剧烈 B.产生的二氧化碳的质量更大 C.参加反应的大理石更多
(4)请从实验原理、原料、发生装置、操作等方面,阐述下列实验中可以产生较平稳气体的主要原因.
| 实验目的 | 原料 | 发生装置 | 主要原因 |
| 制取氧气 | 粉末状二氧化锰和稀过氧化氢溶液 | B |
14. 如图是A、B两种粒子的结构示意图.下列说法正确的是( )
如图是A、B两种粒子的结构示意图.下列说法正确的是( )
 如图是A、B两种粒子的结构示意图.下列说法正确的是( )
如图是A、B两种粒子的结构示意图.下列说法正确的是( )| A. | A、B都不可能是阳离子 | B. | A中x一定是10,B中y一定是7 | ||
| C. | 当y等于8时,B粒子是稳定结构 | D. | 当x等于12时,A是阴离子 |
1.下列仪器的使用或操作准确无误的是( )
| A. |  加热KMnO4制取O2 | B. |  制取蒸馏水 | ||
| C. |  量取浓硫酸 | D. |  加热试管中液体 |
18.由$\stackrel{+1}{H}$、$\stackrel{-2}{O}$、$\stackrel{+4}{C}$、$\stackrel{+2}{Ca}$四种元素按给出的化合价组化合物,最多能组成几种物质( )
| A. | 3种 | B. | 5种 | C. | 7种 | D. | 8种 |
19.比较、推理是化学学习常用的方法,以下是根据一些反应事实推导出的影响化学反应的因素,其中推理不合理的是( )
| 序号 | 化学反应事实 | 影响化学反应的因素 |
| A | 铁钉在10%和20%的稀盐酸中产生气泡的速率不同 | 反应物浓度 |
| B | 碳在常温下不与氧化铜反应,在高温时能与氧化铜反应 | 反应温度 |
| C | 加热氯酸钾反应速率较慢,再加入二氧化锰后迅速分解 | 催化剂 |
| D | 大木桩在空气中很难燃烧,小木条在空气中较易燃烧 | 反应物的种类 |
| A. | A | B. | B | C. | C | D. | D |