题目内容
8.过氧化氢俗称双氧水,常温下是一种无色液体,性质比较稳定.在加热的条件下,它能分解生成氧气和水.查阅资料:
①将新制的浓度5%的双氧水加热到65℃时就有氧气产生,加热到80℃时就有较多氧气产生.
②若在相同质量5%的双氧水加入少量二氧化锰固体,常温下就会立即产生氧气,反应速度快,所需时间短.

请根据图回答问题:
(1)请你写出双氧水和二氧化锰反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.其中二氧化锰的作用是催化作用(或加快双氧水的反应速率).
(2)小晨按图甲装置进行实验,当试管中有大量气泡出现时,伸入带火星的木条,木条并未复燃,为此,他利用图乙装置收集气体,再用带火星的木条检验,木条复燃,那么图甲实验中带火星木条未复燃的原因是加热过氧化氢溶液的同时,溶液中的水蒸气随氧气一起逸出,环境湿度较大,氧气的量较少.
(3)小柯利用催化剂使双氧水分解制制取氧气,若要控制双氧水制取氧气的速率,可以将装置丙作如下改进可将长颈漏斗换为分液漏斗.
(4)采用相同质量5%的双氧水,图丁虚线表示加热分解制取氧气的曲线,请你在该图中用实线画出利用催化剂制取氧气的大致曲线.(假定两种方法过氧化氢均完全分解)
(5)二氧化锰(不溶于水的固体粉末)反应中可以重复使用,理由是二氧化锰的质量和化学性质,在化学反应前后不变;实验结束后可采取的方法,予以回收利用.
(6)如果用图戊的装置收集一瓶氧气,则气体应从n口导入(填“m”或“n”).
分析 (1)根据过氧化氢在二氧化锰催化作用下能分解放出氧气分析;
(2)根据在加热时水受热会蒸发分析;
(3)要控制反应速率,可将长颈漏斗换为分液漏斗.
(4)根据长颈漏斗的使用注意事项分析;
(5)根据催化剂的作用分析解答.
(6)根据氧气的密度比空气的大解答.
解答 解:(1)实验室用过氧化氢溶液和二氧化锰制取氧气的化学方程式是:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,其中二氧化锰的作用是催化作用(或加快双氧水的反应速率);
(2)图甲实验中带火星木条未复燃的原因是:加热过氧化氢溶液的同时,溶液中的水蒸气随氧气一起逸出,环境湿度较大,氧气的量较少;
(3)要控制反应速率,可将长颈漏斗换为分液漏斗.
(4)由于过氧化氢在二氧化锰催化作用下能分解放出氧气,所以,利用催化剂制取氧气的大致曲线为:
(5)二氧化锰(不溶于水的固体粉末)反应中可以重复使用,理由是二氧化锰的质量和化学性质,在化学反应前后不变;实验结束后可采取过滤的方法,予以回收利用.
(6)
故答为:(1)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;催化作用(或加快双氧水的反应速率);
(2)加热过氧化氢溶液的同时,溶液中的水蒸气随氧气一起逸出,环境湿度较大,氧气的量较少;
(3)可将长颈漏斗换为分液漏斗;
(4)
(5)二氧化锰的质量和化学性质,在化学反应前后不变;过滤;
(6)n.
点评 本题较综合的考查了实验室制取氧气的相关知识,认真实验并注重基础知识的积累才能正确解答.熟练掌握实验中选择收集装置和发生装置的依据,其中气体制取装置的选择要看反应物的状态和反应条件;收集装置的选择要看气体的密度和溶水性.

练习册系列答案
相关题目



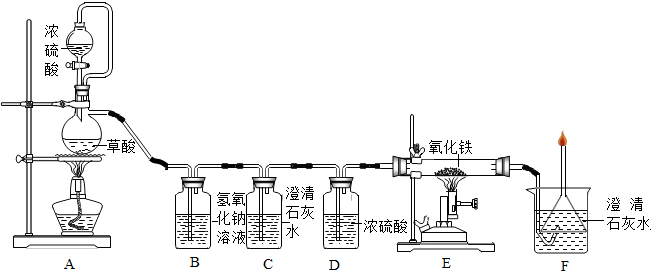 其中A是实验室用草酸(H2C2O4)和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是H2C2O4$\frac{\underline{\;浓H_{2}SO_{4}\;}}{△}$H2O+CO2↑+CO↑.
其中A是实验室用草酸(H2C2O4)和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是H2C2O4$\frac{\underline{\;浓H_{2}SO_{4}\;}}{△}$H2O+CO2↑+CO↑.