题目内容
10.铝、铁、铜是我们生活中常见的金属.(1)铝的利用比铜、铁晚是因为金属大规模开发和利用的先后顺序与A有关(填字母)
A.金属的活动性 B.金属的导电性 C.金属在底壳中的含量
(2)铝具有很好的抗腐蚀性能,原因是通常情况下,铝能够被空气中的氧气氧化,从而在铝表面形成一层保护膜.
(3)每年全世界钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失,铁在空气中锈蚀,实际上是铁跟水和氧气共同作用的结果;防止铁生锈的方法是在铁表面涂一层漆(写一种)
分析 (1)金属越活泼,越不容易冶炼;
(2)铝的化学性质比较活泼;
(3)铁与水和氧气同时接触时容易生锈,根据生锈的条件可以判断防止生锈的方法.
解答 解:(1)铝比铜、铁活泼,开发比较困难,所以开发利用较晚,所以金属开发利用的先后顺序与金属的活动性有关.
故填:A.
(2)通常情况下,铝能够被空气中的氧气氧化,从而在铝表面形成一层保护膜,所以铝具有很好的抗腐蚀性能.
故填:通常情况下,铝能够被空气中的氧气氧化,从而在铝表面形成一层保护膜.
(3)铁在空气中锈蚀,实际上是铁跟水和氧气共同作用的结果.
故填:水;氧气.
在铁表面涂一层漆,或镀一层金属,或把铁制成合金等方法,都能够防止铁生锈.
故填:在铁表面涂一层漆.
答案:
(1)A;
(2)通常情况下,铝能够被空气中的氧气氧化,从而在铝表面形成一层保护膜;
(3)水;氧气;在铁表面涂一层漆.
点评 本题难度不大,掌握金属活动性顺序应用、铁锈蚀的原理等知识是正确解答本题的关键.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
1.N2O能致人发笑,又称“笑气”.其中氮元素的化合价为( )
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
5.2015年我国女科学家屠呦呦发现青蒿素获得诺贝尔医学奖.青蒿素的化学式:C15H22O5,它是一种用于治疗疟疾的药物.下列叙述错误的是( )
| A. | 青蒿素由碳、氢、氧三种元素组成 | |
| B. | 一个青蒿素分子中含42个原子 | |
| C. | 一个青蒿素分子由15个碳原子、22个氢原子和5个氧原子构成 | |
| D. | 青蒿素分子中碳、氢、氧元素的质量比为15:22:5 |
15.关于(NH4)2SO4、NH4Cl、NH4NO3的下列说法中,不正确的是( )
| A. | 与氢氧化钙混合后都有氨气放出 | |
| B. | 都是易溶于水的白色固体 | |
| C. | 可用灼烧的方法来区分出NH4NO3 | |
| D. | 灼烧后(NH4)2SO4、NH4Cl都能燃烧并发亮 |
9.钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量.某补钙药剂说明书的部分信息如图1所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到数据与图象如图2.请根据有关信息回答问题.
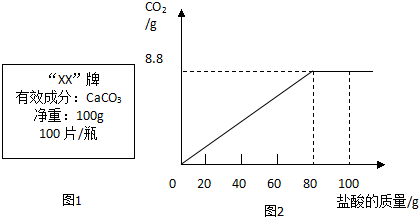
(1)人体缺钙易出现的疾病是骨质疏松,这时除在医生指导下服用保健药剂外,日常生活中要多摄入虾皮或海带或牛奶或骨头汤等等食物.
(2)该品牌补钙药剂中CaCO3的质量分数是50%,a的数值为25.
(3)求该盐酸中溶质的质量分数为(写出计算过程,计算结果保留一位小数).

| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 加入盐酸的质量(g) | 20 | 20 | 20 | 20 | 20 |
| 剩余固体的质量(g) | 35 | 30 | a | 20 | 20 |
(2)该品牌补钙药剂中CaCO3的质量分数是50%,a的数值为25.
(3)求该盐酸中溶质的质量分数为(写出计算过程,计算结果保留一位小数).
10.水是重要的资源,下列说法正确的是( )
| A. | 电解水实验说明水是由氢、氧元素组成的 | |
| B. | 为防止水污染,应禁止使用化肥和农药 | |
| C. | 活性炭能使海水转化为淡水 | |
| D. | 过滤能使硬水转化为软水 |
