题目内容
9.钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量.某补钙药剂说明书的部分信息如图1所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到数据与图象如图2.请根据有关信息回答问题.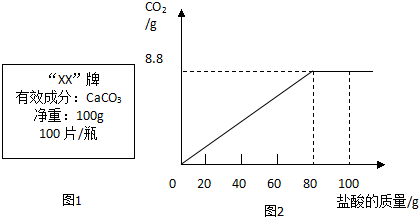
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 加入盐酸的质量(g) | 20 | 20 | 20 | 20 | 20 |
| 剩余固体的质量(g) | 35 | 30 | a | 20 | 20 |
(2)该品牌补钙药剂中CaCO3的质量分数是50%,a的数值为25.
(3)求该盐酸中溶质的质量分数为(写出计算过程,计算结果保留一位小数).
分析 (1)根据缺钙会引起骨质疏松,虾皮或海带或牛奶或骨头汤等含有较多的钙元素解答;
(2)根据二氧化碳的质量结合化学方程式可以计算出碳酸钙的质量即可解答,根据表中数据分析可得a的值;
(3)根据图2可知只有80g盐酸参加反应,根据二氧化碳的质量结合化学方程式可计算80g盐酸中氯化氢的质量即可解答.
解答 解:(1)人体缺钙易出现骨质疏松,日常生活中要多摄入虾皮或海带或牛奶或骨头汤等含有较多的钙元素的食物;
(2)设40片该药剂中含碳酸钙的质量为x,消耗盐酸中的溶质质量为y,
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 73 44
x y 8.8g
$\frac{100}{x}=\frac{73}{y}=\frac{44}{8.8g}$
x=20g,y=14.6g
该品牌补钙药剂中CaCO3的质量分数是:$\frac{20g}{\frac{40片}{100片}×100g}$×100%=50%;
由第1次和第4次数据可知20g稀盐酸可消耗5g碳酸钙,则第二次加入20g稀盐酸后,剩余固体为30g,第三次加入30g稀盐酸后,剩余固体为25g,故a的数值为25;
(3)由表格信息可知,80g稀盐酸与40片药剂中的碳酸钙恰好完全反应,所以该盐酸中溶质的质量分数为:$\frac{14.6g}{80g}$×100%=18.3%;
答案:(1)骨质疏松;虾皮或海带或牛奶或骨头汤等;
(2)50%;25;
(3)反应的盐酸中溶质的质量分数是18.3%.
点评 本题主要考查学生运用化学方程式进行和质量分数公式进行计算的能力.

练习册系列答案
相关题目
7.下列各组物质分别加人足量的水中,能得到无色透明溶液的是( )
| A. | FeCl3、NaOH、NaCl | B. | Na2SO4、HCl、BaCl2 | ||
| C. | MgSO4、NaCl、KOH | D. | K2CO3、NaCl、Na2SO4 |
14.推理是化学学习中常用的思维方法.下列推理正确的是( )
| A. | 碱性溶液能使无色酚酞试液变红,而Na2CO3溶液也能使无色酚酞试液变红,故Na2CO3溶液是 碱性溶液 | |
| B. | CO2、SO2等非金属氧化物能与NaOH溶液反应,则非金属氧化物都能与NaOH溶液反应 | |
| C. | 一定温度下KNO3饱和溶液降低温度会析出晶体,则一定温度下物质的饱和溶液降温都会析出晶体 | |
| D. | 盐是由金属离子和酸根离子构成的,NH4NO3中没有金属离子,不属于盐 |
1.实验盒中有7种没有标签的溶液,老师让化学实验小组同学鉴别这些溶液.
(1)调查研究
①实验盒中记录单上登记的7种溶液是:KMnO4、Na2CO3、CuSO4、NaCl、Ca(OH)2、NaOH和稀盐酸,其中有颜色的是KMnO4、CuSO4溶液.
②查阅资料:无色有刺激性气味的氯化氢气体溶于水得到盐酸.
③研究方式:从5种无色溶液中任意取出4种为一组进行鉴别.这样的组合共有四组.
(2)提出假设:同学们从5种无色溶液中取出4种,贴上A、B、C、D标签,并且假设这一组溶液可能是Na2CO3、NaCl、Ca(OH)2和稀盐酸.
(3)实验探究:同学们按以下步骤进行鉴别.
第一步:取4支试管,分别加入少量的A、B、C、D溶液,然后依次加入少稀盐酸,实验现象记录如下:
实验结论:C是Na2CO3溶液.
第二步:依据如图1装置进行实验,其中夹持固定装置已略去.从长颈漏斗加入稀盐酸,可以观察到C溶液中有气泡产生,A溶液中有白色沉淀生成,B、D溶液均无明显变化.

实验解释:A溶液中发生反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O.
第三步:依据如图2装置进行2个实验.取少量B溶液倒入蒸发皿,加热,闻到有刺激性气味,停止加热.再取少量D溶液倒入另一蒸发皿,加热,有白色固体析出,停止加热.
实验结论:B是稀盐酸,D是NaCl溶液.
经过上述三步实验,同学们认为第5种无色溶液是NaOH溶液.
(4)实验反思:老师引导同学们讨论了上述实验探究过程,进行了全面反思.老师指出:实验结论仍有不确定性.不能确定的是NaCl和NaOH溶液;其鉴别方法是取溶液加入酚酞试液,变红的是氢氧化钠溶液,不变色的是氯化钠溶液.
(1)调查研究
①实验盒中记录单上登记的7种溶液是:KMnO4、Na2CO3、CuSO4、NaCl、Ca(OH)2、NaOH和稀盐酸,其中有颜色的是KMnO4、CuSO4溶液.
②查阅资料:无色有刺激性气味的氯化氢气体溶于水得到盐酸.
③研究方式:从5种无色溶液中任意取出4种为一组进行鉴别.这样的组合共有四组.
(2)提出假设:同学们从5种无色溶液中取出4种,贴上A、B、C、D标签,并且假设这一组溶液可能是Na2CO3、NaCl、Ca(OH)2和稀盐酸.
(3)实验探究:同学们按以下步骤进行鉴别.
第一步:取4支试管,分别加入少量的A、B、C、D溶液,然后依次加入少稀盐酸,实验现象记录如下:
| 溶液 | A | B | C | D |
| 加入盐酸后的现象 | 无明显变化 | 无明显变化 | 有气泡产生 | 无明显变化 |
第二步:依据如图1装置进行实验,其中夹持固定装置已略去.从长颈漏斗加入稀盐酸,可以观察到C溶液中有气泡产生,A溶液中有白色沉淀生成,B、D溶液均无明显变化.

实验解释:A溶液中发生反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O.
第三步:依据如图2装置进行2个实验.取少量B溶液倒入蒸发皿,加热,闻到有刺激性气味,停止加热.再取少量D溶液倒入另一蒸发皿,加热,有白色固体析出,停止加热.
实验结论:B是稀盐酸,D是NaCl溶液.
经过上述三步实验,同学们认为第5种无色溶液是NaOH溶液.
(4)实验反思:老师引导同学们讨论了上述实验探究过程,进行了全面反思.老师指出:实验结论仍有不确定性.不能确定的是NaCl和NaOH溶液;其鉴别方法是取溶液加入酚酞试液,变红的是氢氧化钠溶液,不变色的是氯化钠溶液.