题目内容
13. 溶解度是解决溶液相关问题的重要依据.
溶解度是解决溶液相关问题的重要依据.Ⅰ.根据图1解决下列问题:(M,N均不含结晶水)
(1)温度为t2℃时,M,N两种物质的溶解度相等;
(2)t1℃时,将20gM加入50g水中,充分溶解,形成溶液的质量为65g.保持温度不变,向该溶液中再加入10g水充分搅拌,溶液的溶质质量分数将不变(填“变大”、“变小”或“不变”);
(3)t2℃时,将25gN加入50g水中,完全溶解后要提高该溶液的溶质质量分数,其操作方法是降低温度,再加入N物质.
Ⅱ.根据表格解决实际问题:
| 温度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度/g | KNO3 | 31.6 | 45.8 | 85.5 | 100 | 169 |
| K2CO3 | 110 | 114 | 121 | 126 | 139 | |
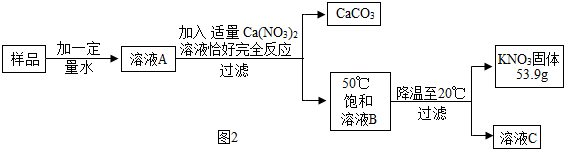
(1)图2中溶液C是饱和(填“饱和”或“不饱和”)溶液;
(2)样品中钾元素的质量为33g(结果保留整数).
分析 根据已有的溶解度曲线的意义进行分析解答,交点表示在同一温度下二者的溶解度相等,根据溶解度曲线确定溶质质量分数的变化;物质提纯时要注意不能生成新的杂质,根据元素的质量计算即可.
解答 解:Ⅰ(1)据图可以看出,在t2℃时M和N的溶解度相等,故填:t2;
(2)t1℃时,M的溶解度是30g,将20gM加入50g水中,充分溶解,只能溶解15g,形成溶液的质量为15g+50g=65g.保持温度不变,向该溶液中再加入10g水充分搅拌,10g水中能溶解M3g,故仍然是饱和溶液,溶液的溶质质量分数将不变,故填:65,不变;
(3)t2℃时,N的溶解度是50g,将25gN加入50g水中,完全溶解形成的是饱和溶液,要提高该溶液的溶质质量分数,可以降低温度,再加入N物质,故填:降低温度,再加入N物质;
Ⅱ.(1)加入硝酸钙溶液,硝酸钙与碳酸钾反应生成碳酸钙沉淀和硝酸钾,故B是硝酸钾的饱和溶液,降温析出晶体,溶液C是硝酸钾的饱和溶液,故图2中溶液C是饱和溶液,故填:饱和;
(2)50℃时硝酸钾的溶解度是85.5g,20℃时硝酸钾的溶解度是31.6g,析出晶体是53.9g,恰好是100g水中析出的硝酸钾的质量,故溶液C中水的质量是100g,其中硝酸钾的质量是31.6g,故硝酸钾的质量是53.9g+31.6g=85.5g,样品中钾元素的质量为85.5g×$\frac{39}{101}$≈33g,故填:33.
点评 本题考查的是溶解度曲线的应用,完成此题,可以依据已有的溶解度曲线的意义进行.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.2015年4月6日晚19时左右,位于福建漳州的古雷PX项目突然发生爆炸,这是该项目两年内第二次发生爆炸.PX的中文名称为对二甲苯,化学式为C8H10,无色透明液体,不溶于水,具有芳香气味,且稳定,可燃,属低毒化合物,其蒸气与空气可形成爆炸性混合物,爆炸极限1.1%~7.0%(体积分数).关于PX的说法正确的是( )
| A. | 对二甲苯的化学性质稳定,具有可燃性 | |
| B. | 对二甲苯中碳氢元素的质量比为4:5 | |
| C. | 对二甲苯是由碳原子和氢原子构成 | |
| D. | 对二甲苯属于剧毒物质 |
8.根据 这4种微粒结构示意图,判断下列说法中正确的是( )
这4种微粒结构示意图,判断下列说法中正确的是( )
 这4种微粒结构示意图,判断下列说法中正确的是( )
这4种微粒结构示意图,判断下列说法中正确的是( )| A. | 它们都带有电荷 | B. | 它们表示同一种元素 | ||
| C. | 它们核外电子排布相同 | D. | 它们都具有相对稳定结构 |
5.下列变化中属于化学变化的是( )
| A. | 金块抽成金线 | B. | 干冰升华 | C. | 可燃冰燃烧 | D. | 蔗糖溶解于水 |
2.下列标志属于物品回收标志的是( )
| A. |  | B. |  | C. |  | D. |  |
3.下列除去杂质所用的药品或方法,不正确的是( )
| 选项 | 物 质 | 杂 质 | 除杂药品或方法 |
| A | CaCl2溶液 | 盐酸 | 过量的碳酸钙、过滤 |
| B | CaO | CaCO3 | 适量稀盐酸 |
| C | N2 | O2 | 灼热的铜网 |
| D | CO | CO2 | 足量的氢氧化钠溶液、浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |

 兰州市中山桥南侧的“将军柱”(铸造材质主要是铁),距今已有630年的历史,它与中山桥一起组成了“兰州铁路”一景,近日“将军柱”商标获得国家批准.
兰州市中山桥南侧的“将军柱”(铸造材质主要是铁),距今已有630年的历史,它与中山桥一起组成了“兰州铁路”一景,近日“将军柱”商标获得国家批准.