题目内容
19.12gA和足量B混合加热至完全反应,生成8gC和6gD,则参加反应的A与B的质量比是( )| A. | 5:1 | B. | 4:3 | C. | 6:1 | D. | 2:1 |
分析 由题意可知,反应物是A和B,生成物是C和D,根据质量守恒定律可以求出参加反应的B的质量,进而求出参加反应的A和B的质量比.
解答 解:12gA和足量B混合加热至完全反应后生成8gC和6gD,由质量守恒定律可知,参加反应的B的质量为8g+6g-12g=2g,故参加反应的A和B的质量比是12g:2g=6:1.
故选:C.
点评 本题解题的关键是运用化学中的基本思想:质量守恒思想.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
10.小明和小亮同学在实验室帮老师配制石灰水时,将两药匙熟石灰样品放入小烧杯中,向其中加入一定量的蒸馏水,充分搅拌后发现烧杯底部仍有不溶性的固体,于是小明认为熟石灰样品已经变质.小亮同学不同意他的判断,小亮同学的理由是氢氧化钙微溶于水,固体可能是氢氧化钙.同学们针对该熟石灰样品的成分展开了讨论,请你参与讨论并完成实验报告.
【提出问题】熟石灰样品的主要成分是什么?
【作出猜想】甲同学猜想是Ca(OH)2;乙同学猜想是CaCO3,你的猜想是Ca(OH)2和CaCO3.
【实验与结论】请你通过实验验证你的猜想:
【提出问题】熟石灰样品的主要成分是什么?
【作出猜想】甲同学猜想是Ca(OH)2;乙同学猜想是CaCO3,你的猜想是Ca(OH)2和CaCO3.
【实验与结论】请你通过实验验证你的猜想:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量的熟石灰样品于烧杯中,加适量的水充分溶解后过滤. (1)向滤液中加入适量的酚酞溶液; | 溶液变红; | 样品中有Ca(OH)2 |
| (2)向滤出固体中加入适量稀盐酸溶液. | 产生气体. | 样品中有CaCO3 |
7.地壳中含量最多的金属元素可以表示为( )
| A. | O | B. | Si | C. | Ca | D. | Al |
14.下列反应中,元素化合价在反应前后都没有发生改变的是( )
| A. | SO2+2NaOH=Na2SO3+H2O | B. | C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ | ||
| C. | 2Na+2H2O=2NaOH+H2↑ | D. | Mg+Cl2$\frac{\underline{\;点燃\;}}{\;}$MgCl2 |
11.下列图示实验操作中,正确的是( )
| A. |  读出液体体积 | B. |  过滤 | C. |  用滴管滴加液体 | D. |  加热液体 |
8.下列物质中属于纯净物的是( )
| A. | 干冰 | B. | 空气 | C. | 海水 | D. | 石油 |
9.下列四个图象中,能正确表示对应变化关系的是( )
| A. | 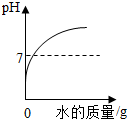 向一定量稀盐酸中加水稀释 | |
| B. | 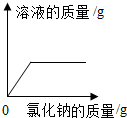 一定温度下,向不饱和食盐水中加入氯化钠 | |
| C. |  加热一定量的高锰酸钾固体 | |
| D. | 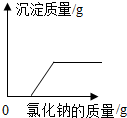 向硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液 |
 在元素周期表中,元素的周期数与原子核外的电子层数相同.如图是某元素的粒子结构示意图,则该元素的周期数为( )
在元素周期表中,元素的周期数与原子核外的电子层数相同.如图是某元素的粒子结构示意图,则该元素的周期数为( )