题目内容
15. 如图所示的是几种常见物质的转化关系.A-H及甲、乙分别表示不同物质,D为刺激性气味气体,E是生产、生活中应用量最大的金属单质,乙可用于中和酸性土壤;反应①为化合反应(部分反应物、生成物及反应条件已略).请回答下列问题:
如图所示的是几种常见物质的转化关系.A-H及甲、乙分别表示不同物质,D为刺激性气味气体,E是生产、生活中应用量最大的金属单质,乙可用于中和酸性土壤;反应①为化合反应(部分反应物、生成物及反应条件已略).请回答下列问题:(1)C的化学式为N2.
(2)反应②的化学方程式为Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2(写一个),该反应在实际生产中可用于冶炼金属.
(3)图中物质一定属于氧化物的是甲、F、H(用图中文字或字母表示).
分析 电解水生成氢气和氧气,氢气和氮气在一定条件下反应生成氨气,氨气具有刺激性气味,氢氧化钙可以用来改良酸性土壤,能和硫酸铵反应生成硫酸钙、水和氨气;
铁是生产、生活中应用量最大的金属单质,在氧气中燃烧生成四氧化三铁,高温条件下,四氧化三铁能和碳、一氧化碳等物质反应生成铁和二氧化碳.
解答 解:电解水生成氢气和氧气,氢气和氮气在一定条件下反应生成氨气,氨气具有刺激性气味,氢氧化钙可以用来改良酸性土壤,能和硫酸铵反应生成硫酸钙、水和氨气;
铁是生产、生活中应用量最大的金属单质,在氧气中燃烧生成四氧化三铁,高温条件下,四氧化三铁能和碳、一氧化碳等物质反应生成铁和二氧化碳,因此甲、乙、A、B、C、D、E、F、G、H分别是水、氢氧化钙、氢气、氧气、氮气、氨气、铁、四氧化三铁、碳或一氧化碳、二氧化碳;
(1)C是氮气,氮气的化学式为N2.
故填:N2.
(2)反应②中,四氧化三铁能和一氧化碳在高温条件下反应生成铁和二氧化碳,反应的化学方程式为:
Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2,该反应在实际生产中可用于冶炼金属.
故填:Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2;冶炼金属.
(3)图中物质一定属于氧化物的是水、四氧化三铁、二氧化碳.
故填:甲、F、H.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.我市某校初三(1)班学生去湖光岩春游,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分数相同的盐酸与样品充分反应来讲行实验测定,(样品中的杂质不溶于水,且不与盐酸反应),测得数据如表:
试问答:
(1)10.0g样品与45g盐酸充分反应后,盐酸是否还剩余否 (填“是”或“否”),样品中碳酸钙的质量分数是90%.
(2)求出四位同学所用稀盐酸的溶质质量分数.
| 甲同学 | 乙同学 | 丙同学 | 丁同学 | |
| 所取石灰石样品质量(g) | 10.0 | 10.0 | 10.0 | 10.0 |
| 加入盐酸的质量(g) | 20.0 | 30.0 | 45.0 | 50.0 |
| 剩余固体的质量(g) | 6.0 | 4.0 | 1.0 | 1.0 |
(1)10.0g样品与45g盐酸充分反应后,盐酸是否还剩余否 (填“是”或“否”),样品中碳酸钙的质量分数是90%.
(2)求出四位同学所用稀盐酸的溶质质量分数.
10.空气是人类宝贵的自然资源,下列关于空气的说法错误的是( )
| A. | 空气的主要成分是氮气(78%)和氧气(21%) | |
| B. | 造成空气污染的气体主要有CO、CO2和SO2等 | |
| C. | 饼干在空气中变软是因为空气中含有水蒸气 | |
| D. | 根据沸点不同,工业上常用分离液态空气的方法制备氧气 |
2.如图所示实验操作中正确的是( )
| A. |  倾倒液体 | B. |  读取量筒里液体体积 | ||
| C. |  熄灭酒精灯 | D. |  向试管内加固体粉末 |
9.如图为元素周期表的一部分,下列说法错误的是( )


| A. | 碳的相对原子质量为12.01 | B. | 氮原子的核外电子数为7 | ||
| C. | 氧元素只能形成一种单质 | D. | C、N、O的原子序数依次增加 |
7.某密闭容器中有 X、O2和 CO2三种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表.请根据表中信息,判断下列说法正确的是( )
| 物质 | X | O2 | CO2 | H2O |
| 反应前各物质质量 | 23 | 70 | 1 | 0 |
| 反应后各物质质量 | 0 | 待测 | 45 | 27 |
| A. | 表中“待测”值为 21 | |
| B. | 该反应为分解反应 | |
| C. | X 中含有氧元素 | |
| D. | 反应生成的 CO2和 H2O 质量比为 45:27 |
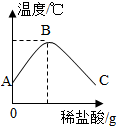 将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示:
将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示:
 如图中的A-I表示几种初中化学常见的纯净物,且分别是由H、C、O、S、Cl、Na、Ca中的两种或两种以上元素组成.其中A、E、H是氧化物;A中氧元素质量分数为50%;I俗称小苏打,C、I分别与足量F反应的生成物相同.图中“--”表示两端的物质问能发生化学反应;“一”表示物质间存在转化关系:部分反应物或生成物已略去.
如图中的A-I表示几种初中化学常见的纯净物,且分别是由H、C、O、S、Cl、Na、Ca中的两种或两种以上元素组成.其中A、E、H是氧化物;A中氧元素质量分数为50%;I俗称小苏打,C、I分别与足量F反应的生成物相同.图中“--”表示两端的物质问能发生化学反应;“一”表示物质间存在转化关系:部分反应物或生成物已略去.