题目内容
11.(1)过氧化钠(Na2O3)是潜水艇中的制氧剂,它能与二氧化碳反应生成氧气和另一种常见化合物,请写出此反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2;在过氧化钠中氧元素的化合价为-1.(2)二氧化硅属于非金属氧化物.它的结构与金刚石相似,都是由原子(填“分子”、“原子”或“离子”)构成的.装有氢氧化钠溶液的试剂瓶不能用玻璃塞,原因是在常温下,NaOH与玻璃塞中的SiO2缓慢地发生反应生成Na2SiO3,Na2SiO2使瓶口与瓶塞粘合在一起,该反应的化学方程式为2NaOH+SiO2=Na2SiO3+H2O.
(3)氢氧化钠具有强烈的腐蚀性,如果不慎沾到皮肤上,要用大量的水冲洗,再涂上硼酸(H3BO3)溶液,请写出该反应的化学方程式3NaOH+H3BO3═Na3BO3+3H2O.
分析 (1)过氧化钠与二氧化碳反应生成碳酸钠和氧气,写出反应的化学方程式即可.
根据在化合物中正负化合价代数和为零,进行分析解答.
(2)根据题意,二氧化硅属于非金属氧化物,它的结构与金刚石相似;NaOH与玻璃塞中的SiO2缓慢地发生反应生成Na2SiO3,同时生成水,进行分析解答.
(3)氢氧化钠与硼酸(H3BO3)溶液反应生成硼酸钠和水,写出反应的化学方程式即可.
解答 解:(1)过氧化钠固体与二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2.
钠元素显+1价,设氧元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+2x=0,则x=-1价.
(2)二氧化硅属于非金属氧化物,它的结构与金刚石相似,金刚石属于固态非金属单质,是由碳原子直接构成的,则二氧化硅是由原子构成的.
NaOH与玻璃塞中的SiO2缓慢地发生反应生成Na2SiO3,同时生成水,反应的化学方程式为:2NaOH+SiO2=Na2SiO3+H2O.
(3)氢氧化钠与硼酸(H3BO3)溶液反应生成硼酸钠和水,反应的化学方程式为:3NaOH+H3BO3═Na3BO3+3H2O.
故答案为:(1)2Na2O2+2CO2=2Na2CO3+O2;-1;(2)原子;2NaOH+SiO2=Na2SiO3+H2O;(3)3NaOH+H3BO3═Na3BO3+3H2O.
点评 本题难度不大,掌握化学方程式的书写方法、化合价的原则、物质的微观构成等是正确解答本题的关键.

练习册系列答案
相关题目
2.关于溶液的下列叙述中,正确的是( )
| A. | 溶液都是无色透明的液体 | B. | 蔗糖溶液能导电 | ||
| C. | 溶液一定是混合物 | D. | 溶液中的溶质只可以是固体 |
6.下列反应中,属于缓慢氧化的是( )
| A. | 煤燃烧 | B. | 食物腐败 | C. | 车胎爆炸 | D. | 高锰酸钾制氧气 |
16.下列厨房用具,在空气中最容易锈蚀的是( )
| A. | 铝壶 | B. | 不锈钢汤勺 | C. | 铁锅 | D. | 纯铜把手 |
 氨气(NH3)有强烈的刺激性气味,密度比空气小,具有还原性,在纯氧中能够认识,当与空气混合时(在爆炸极限范围内),通明火也能发生爆炸.如图是验证NH3在加热条件下具有还原性的装置,当挤压橡皮球把氩气鼓入盛有浓氨水的广口瓶时,就能促使氨水挥发出NH3并进入试管,请回答下列问题:
氨气(NH3)有强烈的刺激性气味,密度比空气小,具有还原性,在纯氧中能够认识,当与空气混合时(在爆炸极限范围内),通明火也能发生爆炸.如图是验证NH3在加热条件下具有还原性的装置,当挤压橡皮球把氩气鼓入盛有浓氨水的广口瓶时,就能促使氨水挥发出NH3并进入试管,请回答下列问题:

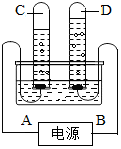 水是我们生活中重要物质.请用学过的知识回答下列有关水的问题:
水是我们生活中重要物质.请用学过的知识回答下列有关水的问题: 碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小红同学设计实验对碳酸氢钠的性质进行了探究.请你参与她的探究活动.
碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小红同学设计实验对碳酸氢钠的性质进行了探究.请你参与她的探究活动.