题目内容
通过一年的化学学习,我们认识了“酸”、“碱”、“盐”,请回答下列问题:
(1)常见的酸有硫酸、盐酸等,在它们的水溶液里由于存在有相同的 (填符号),因此,它们有很多相似的化学性质;
(2)常见的碱有氢氧化钠、氢氧化钙等,氢氧化钙可由生石灰与水反应制得,反应的化学方程式为 .
(3)碳酸氢钠是一种常见的盐,可治疗胃酸过多症.被人服用后与胃酸反应,该反应的化学方程式为 .
(4)中和反应在日常生活和工农业生产中有广泛的应用,如硫酸厂的污水中含有硫酸等杂质,可用熟石灰进行处理,反应的化学方程式为 .
(1)常见的酸有硫酸、盐酸等,在它们的水溶液里由于存在有相同的
(2)常见的碱有氢氧化钠、氢氧化钙等,氢氧化钙可由生石灰与水反应制得,反应的化学方程式为
(3)碳酸氢钠是一种常见的盐,可治疗胃酸过多症.被人服用后与胃酸反应,该反应的化学方程式为
(4)中和反应在日常生活和工农业生产中有广泛的应用,如硫酸厂的污水中含有硫酸等杂质,可用熟石灰进行处理,反应的化学方程式为
考点:酸的化学性质,生石灰的性质与用途,中和反应及其应用,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的酸 酸的通性,常见的碱 碱的通性,常见的盐 化学肥料
分析:(1)理解酸的定义:酸是在水溶液中电离出的阳离子全部是氢离子的化合物.熟记酸的通性.
(2)根据反应物、生成物和条件.
(3)碳酸氢钠与HCl反应生成氯化钠、水和二氧化碳,可以治疗胃酸过多;
(4)根据硫酸与氢氧化钙的反应写出反应的方程式.
(2)根据反应物、生成物和条件.
(3)碳酸氢钠与HCl反应生成氯化钠、水和二氧化碳,可以治疗胃酸过多;
(4)根据硫酸与氢氧化钙的反应写出反应的方程式.
解答:解:(1)因为酸是在水溶液中电离出的阳离子全部是氢离子的化合物,所以酸在水溶液中具有相同的H+,故填H+;
(2)生石灰与水反应生成氢氧化钙:CaO+H2O═Ca(OH)2;
(3)碳酸氢钠具有弱碱性,与HCl反应生成氯化钠、水和二氧化碳,反应的化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑,故可以治疗胃酸过多,
(4)硫酸与氢氧化钙的反应生成了硫酸钙和水,反应的方程式是:Ca(OH)2+H2SO4═CaSO4+2H2O.
故答案为:(1)H+(2)CaO+H2O=Ca(OH)2(3)NaHCO3+HCl=NaCl+H2O+CO2↑
(4)H2SO4+Ca(OH)2=CaSO4+2H2O
(2)生石灰与水反应生成氢氧化钙:CaO+H2O═Ca(OH)2;
(3)碳酸氢钠具有弱碱性,与HCl反应生成氯化钠、水和二氧化碳,反应的化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑,故可以治疗胃酸过多,
(4)硫酸与氢氧化钙的反应生成了硫酸钙和水,反应的方程式是:Ca(OH)2+H2SO4═CaSO4+2H2O.
故答案为:(1)H+(2)CaO+H2O=Ca(OH)2(3)NaHCO3+HCl=NaCl+H2O+CO2↑
(4)H2SO4+Ca(OH)2=CaSO4+2H2O
点评:主要考查了酸的化学性质、酸碱性的测定相关的知识,培养学生的应用知识的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列物质的分类,对应正确的是( )
| A、混合物:水银、天然气 |
| B、新能源:太阳能、潮汐能 |
| C、合成材料:合金、塑料 |
| D、碳单质:金刚石、石灰石 |
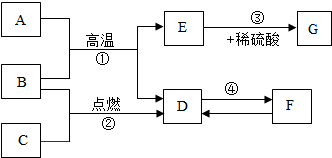 如图A~G是初中化学常见的物质,其中A为红棕色固体,E为固体单质,B、C、D均为无色气体,F为石灰石的主要成分,G为浅绿色溶液,各物质的转化关系见图,请根据图回答下列问题.
如图A~G是初中化学常见的物质,其中A为红棕色固体,E为固体单质,B、C、D均为无色气体,F为石灰石的主要成分,G为浅绿色溶液,各物质的转化关系见图,请根据图回答下列问题. 实验是学习化学的重要手段,通过实验可以培养实践能力和创新精神.
实验是学习化学的重要手段,通过实验可以培养实践能力和创新精神.