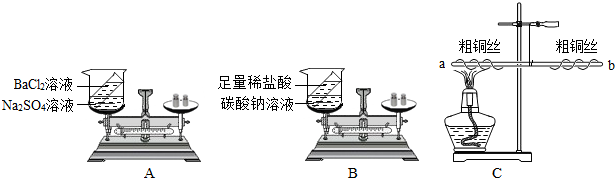
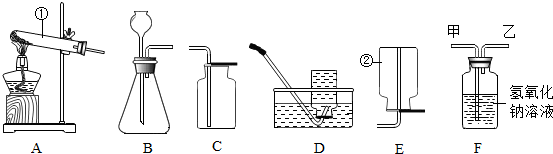
题目内容
2.用I2O5可测定空气受CO污染的程度,发生反应的化学方程式如下:I2O5+5CO$\frac{\underline{\;\;△\;\;}}{\;}$I2+5CO2,根据生成CO2的多少,可以判断CO的含量,关于这个反应,下列说法正确的是( )| A. | 参加反应的I2O5的质量等于生成物I2的质量 | |
| B. | 参加反应的各物质中的氧原子总数等于生成物CO2中的氧原子总数 | |
| C. | 反应物所含元素种类与生成物所含元素种类相同,各原子数目不相等 | |
| D. | 参加反应的I2O5和CO的质量比等于生成的I2和CO2的质量比 |
分析 A、根据参加反应的物质的质量和等于生成物质的质量和进行分析;
B、根据化学反应前后原子的个数不变进行分析;
C、根据反应前后的元素种类不变进行分析;
D、根据质量守恒定律进行分析.
解答 解:A、参加反应的物质质量和等于生成物的质量和,但是某种反应物的质量不一定等于生成物的质量,故A错误;
B、根据质量守恒定律可知,化学反应前后原子个数不变,故B正确;
C、在化学反应前后各原子数目相等,故C错误;
D、参加反应的物质质量和等于生成物的质量和,但是质量比不一定相等,故D错误.
故选:B.
点评 在解此类题时,首先分析题中的反应原理,然后利用质量守恒定律的相关知识进行分析解答.

练习册系列答案
相关题目
13.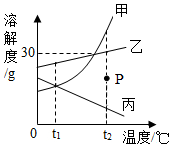 如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
 如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )| A. | t1℃时,甲、丙两种物质的溶液中溶质的质量分数一定相等 | |
| B. | t1℃将15g的乙物质加到50g水中充分溶解可得到65g的饱和溶液 | |
| C. | 将P点甲物质的溶液变为饱和溶液只能通过向溶液中增加甲物质的方法来实现 | |
| D. | 将t1℃时三种物质的饱和溶液温度升高到t2℃,所得溶液中溶质的质量分数由大到小的顺序为:乙>甲>丙 |
14.水是生命的源泉,也是不可缺少的资源.
(1)某矿泉水的主要矿物质成分机及含量如表,这里Ca、K、Zn、F是指元素.(填“单质、元素、分子或原子”)
(2)水污染日益严重,水资源的保护和合理利用已受到人们的普遍关注,请参与讨论下列有关问题:
(Ⅰ)自来水、冰水混合物、海水中属于纯净物的是冰水混合物.
(Ⅱ)某学校饮水处可以将自来水净化为饮用水,其中处理步骤如图所示:
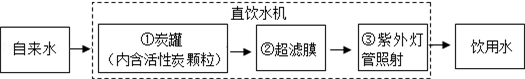
①对应的作用是B(填字母序号,下同).
A.杀菌消毒 B.吸附杂质 C.沉淀过滤 D.蒸馏
(Ⅲ)下列做法会造成水体污染的有AD.
A、工业废水直接排放 B、工业废气处理后排放
C、禁止使用含磷洗衣粉 D、大量使用化肥、农药
(Ⅳ)能确认水是由氧元素和氢元素组成的实验是AC.
A、氢气在氧气中燃烧生成水 B、水的蒸发 C、水的电解 D、水的净化
(3)长期饮用硬水可能会引起体内结石,鉴别硬水和软水最简单的方法是用肥皂水鉴别.
(4)水通电分解生成最理想的能源--氢气,电解一定量的水,当其中负极产生5ml气体时,正极产生的气体体积是2.5ml.
(1)某矿泉水的主要矿物质成分机及含量如表,这里Ca、K、Zn、F是指元素.(填“单质、元素、分子或原子”)
| 成分 | Ca | K | Zn | F |
| 含量(mg/L) | 20 | 3 | 0.06 | 0.02 |
(Ⅰ)自来水、冰水混合物、海水中属于纯净物的是冰水混合物.
(Ⅱ)某学校饮水处可以将自来水净化为饮用水,其中处理步骤如图所示:

①对应的作用是B(填字母序号,下同).
A.杀菌消毒 B.吸附杂质 C.沉淀过滤 D.蒸馏
(Ⅲ)下列做法会造成水体污染的有AD.
A、工业废水直接排放 B、工业废气处理后排放
C、禁止使用含磷洗衣粉 D、大量使用化肥、农药
(Ⅳ)能确认水是由氧元素和氢元素组成的实验是AC.
A、氢气在氧气中燃烧生成水 B、水的蒸发 C、水的电解 D、水的净化
(3)长期饮用硬水可能会引起体内结石,鉴别硬水和软水最简单的方法是用肥皂水鉴别.
(4)水通电分解生成最理想的能源--氢气,电解一定量的水,当其中负极产生5ml气体时,正极产生的气体体积是2.5ml.