题目内容
2.学习了二氧化锰对过氧化氢分解有催化作用的知识后,某同学想:氧化铜能否起到类似二氧化锰的催化剂作用呢?于是进行以下探究.【猜想】Ⅰ、氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、氧化铜参与反应产生氧气,反应前后质量和化学性质发生了改变;
Ⅲ、氧化铜是反应的催化剂,反应前后质量和化学性质不变.
【实验】用天平称量0.2g氧化铜(CuO),取5mL5%的过氧化氢溶液于试管中,
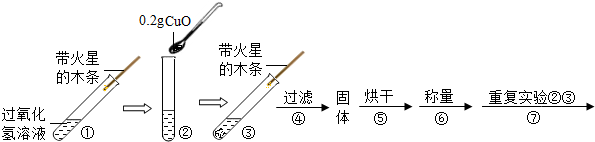
进行实验:
(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 有气泡产生, 带火星的木条复燃 | 称量的氧化铜的质量仍为0.2g | 溶液中有气泡, 带火星的木条复燃. | 猜想Ⅰ、Ⅱ不成立;猜想Ⅲ成立. |
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒.所缺仪器在此步骤中的作用是引流.
(4)过氧化氢能被氧化铜催化分解放出氧气的化学方程为2H2O2$\frac{\underline{\;氧化铜\;}}{\;}$2H2O+O2↑.
分析 【猜想】根据催化剂的定义回答.
【实验】(1)根据氧化铜对过氧化氢的分解有催化作用回答③现象;根据催化剂的定义和特点回答⑥结果;根据催化剂的定义和特点回答⑦现象.
(2)根据对比实验的探究方法回答.
(3)根据过滤的操作过程回答,要注意仪器与材料或用品不同.
(4)过氧化氢分解产生了水和氧气,可以据此写出该反应的化学方程式.
解答 解:【猜想】催化剂的特点是“一变,两不变”,即反应速率变,质量和化学性质不变.
【实验】(1)氧化铜对过氧化氢的分解有催化作用,能加快其分解速率生成氧气的速率,故步骤③中的现象是有气泡产生,带火星的木条复燃;催化剂的特点是“一变,两不变”,反应前后其质量不变,所以步骤⑥中称量的氧化铜的质量仍为0.2g;催化剂的特点是“一变,两不变”,其中反应速率改变,这里是加快,所以⑦的现象是溶液中有气泡放出,带火星的木条复燃.
(2)为了看氧化铜是否能改变反应的速率,要通过加入氧化铜与不加氧化铜的现象进行对比,才能得出科学合理的结论.
(3)过滤用到的仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒,缺少最后一种,其作用为引流.
(4)过氧化氢在氧化铜的催化作用之下分解产生了水和氧气,化学方程为2H2O2$\frac{\underline{\;氧化铜\;}}{\;}$2H2O+O2↑.
故答案为:【猜想】质量和化学性质不变;
【实验】(1)
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 有气泡产生带火星的木条复燃 | 称量的氧化铜的质量仍为0.2g | 溶液中有气泡放出 带火星的木条复燃 | 猜想Ⅰ、Ⅱ不成立;猜想Ⅲ成立. |
(3)玻璃棒;引流.
(4)2H2O2$\frac{\underline{\;氧化铜\;}}{\;}$2H2O+O2↑.
点评 催化剂、催化作用是初中重要基本概念之一,是考查的重点和热点,主要考查对催化剂、催化作用概念的理解,对催化效率影响因素的探究等.

练习册系列答案
相关题目
12.何家坝柚子是蓬溪特产之一,个大,皮香味浓郁,油色光亮,柚顶有七条放射沟,其味香甜略带酸,细嫩化渣.能闻到柚子的香味是因为( )
| A. | 分子在不断运动 | B. | 分子间有间隔 | C. | 分子体积很小 | D. | 分子质量很小 |
10.在下列表中填上符合要求的化学符号或名称
| 符号名称 | 亚铁离子 | 二氧化氮中氮元素为+4价 | 氖气 | 七氧化二氯 |
| 化学符号 | Fe2+ | $\stackrel{+4}{N}$O2 | Ne | Cl2O7 |
17.下列实验方案中,不能达到实验目的是( )
| A. | 鉴别硬水和软水----加肥皂水搅拌 | |
| B. | 除去氯化钠固体中的少量碳酸钠----加入适量稀盐酸,充分反应后,蒸发 | |
| C. | 分离碳酸钠和氢氧化钠的混合物----加入过量氯化钙溶液,过滤 | |
| D. | 区分羊毛与合成纤维----点燃,闻气味 |
14.下列关于CO和CO2的叙述正确的是( )
| A. | CO和CO2均具有可燃性 | |
| B. | CO和CO2均能与H2O反应 | |
| C. | CO和CO2的密度均大于空气的密度 | |
| D. | CO和CO2在一定条件下可以相互转化 |
12.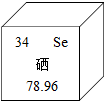 硒对人体有防癌、抗癌作用.如图是硒元素在元素周期表中的部分信息,下列有关说法正确的是( )
硒对人体有防癌、抗癌作用.如图是硒元素在元素周期表中的部分信息,下列有关说法正确的是( )
 硒对人体有防癌、抗癌作用.如图是硒元素在元素周期表中的部分信息,下列有关说法正确的是( )
硒对人体有防癌、抗癌作用.如图是硒元素在元素周期表中的部分信息,下列有关说法正确的是( )| A. | 硒属于金属元素 | B. | 硒的原子序数是34 | ||
| C. | 硒原子核内中子数是34 | D. | 硒的相对原子质量是78.96g |
 生活离不开水.净化水的知识在日常生活中有着广泛的应用.
生活离不开水.净化水的知识在日常生活中有着广泛的应用.